Questões de Vestibular
Foram encontradas 584 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!

O princípio de funcionamento dessa espécie de ar-condicionado baseia-se no fato de o gelo sofrer uma
Considere o diagrama energético de uma reação:
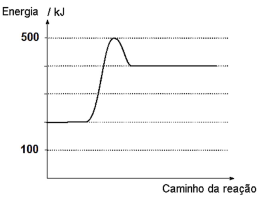
A energia de ativação e a variação de entalpia da reação são, respectivamente, iguais a:
Em 2011 celebramos o Ano Internacional da Química. Além disso, 2011 é também o ano do centenário do recebimento do Prêmio Nobel de Química por Marie Curie, que foi a primeira cientista a receber dois Prêmios Nobel, o primeiro em 1903, em Física, devido às suas contribuições para as pesquisas em radioatividade, e o segundo em 1911, pela descoberta dos elementos rádio e polônio. O polônio não possui isótopos estáveis, todos são radioativos, dos quais apenas o 210Po ocorre naturalmente, sendo gerado por meio da série de decaimento do rádio. A seguir são ilustrados dois trechos da série de decaimento do rádio:
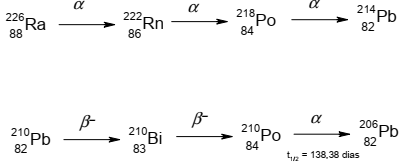
Com base nas informações fornecidas, considere as seguintes afirmativas:
1. A partícula α possui número de massa igual a 4.
2. Para converter 214Pb em 210Pb, conectando os dois trechos da série, basta a emissão de uma partícula α.
3. Uma amostra de 210Po será totalmente convertida em 206Pb após 276,76 dias.
4. No decaimento β − , o número de massa é conservado, pois um nêutron é convertido em um próton.
Assinale a alternativa correta.
Algumas bactérias do solo, como as nitrobactérias, catalisam a oxidação do nitrogênio contido em sais de amônio (fertilizante químico) formando nitrato, o qual pode ser assimilado pelos vegetais.
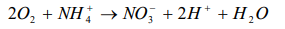
É correto afirmar que o nitrogênio presente no
ânion nitrato apresenta um número de oxidação
(Nox) de:
Observe a reação abaixo, que representa a adição de uma solução de permanganato de potássio em uma solução de ácido clorídrico.
KMnO4(aq) + HCI(aq) → KCI(aq) + MnCI2(aq) + CI2(g) + H2O(I)
O coeficiente estequiométrico do ácido clorídrico
da reação balanceada é