Questões de Vestibular
Foram encontradas 451 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
A pilha seca tem potencial padrão de 1,5 V e consiste de um anodo de zinco e um catodo de dióxido de manganês. O meio eletrolítico é uma pasta umedecida contendo carvão, cloreto de amônio e cloreto de zinco. A equação química da reação espontânea que ocorre da pilha é a seguinte:
Zn(s) + 2 MnO2(aq) + 2 NH4 + (aq) → Zn2+(aq) + Mn2 O3(s) + 2 NH3(g) + H2 O(aq)
A variação no valor de Nox na semirreação de redução é de
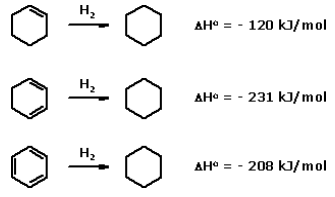
A diferença nas entalpias de hidrogenação das reações apresentadas pode ser explicada pela