Questões de Vestibular
Foram encontradas 706 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Ao final da mortandade, a quantidade consumida, em quilogramas, de gás oxigênio dissolvido foi igual a:
O craqueamento é uma reação química empregada industrialmente para a obtenção de moléculas mais leves a partir de moléculas mais pesadas. Considere a equação termoquímica abaixo, que representa o processo utilizado em uma unidade industrial para o craqueamento de hexano.
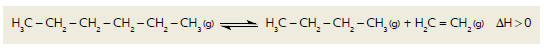
Em um experimento para avaliar a eficiência desse processo, a reação química foi iniciada sob
temperatura T1
e pressão P1
. Após seis horas, a temperatura foi elevada para T2 , mantendo-se a
pressão em P1
. Finalmente, após doze horas, a pressão foi elevada para P2 , e a temperatura foi
mantida em T2
.
A variação da concentração de hexano no meio reacional ao longo do experimento está
representada em:
O monóxido de carbono, formado na combustão incompleta em motores automotivos, é um gás extremamente tóxico. A fim de reduzir sua descarga na atmosfera, as fábricas de automóveis passaram a instalar catalisadores contendo metais de transição, como o níquel, na saída dos motores.
Observe a equação química que descreve o processo de degradação catalítica do monóxido de carbono:
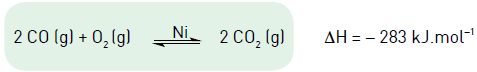
Com o objetivo de deslocar o equilíbrio dessa reação, visando a intensificar a degradação catalítica do monóxido de carbono, a alteração mais eficiente é:
HCN (aq) ⇔ H+ (aq) + CN– (aq)
Um experimento sobre esse equilíbrio químico, realizado a temperatura constante, analisou quatro parâmetros, apresentados na tabela:
Parâmetro: grau de ionização
Símbolo: α
Parâmetro: constante de equilíbrio
Símbolo: Ka
Parâmetro: potencial hidrogeniônico
Símbolo: pH
Parâmetro: concentração de HCN
Símbolo: [HCN]
Ao ser estabelecido o equilíbrio químico da ionização, foi adicionada certa quantidade de NaCN(s). Após a dissolução e dissociação completa desse composto, houve deslocamento do equilíbrio de ionização.
O parâmetro que sofreu redução, após a adição do composto, é representado pelo seguinte símbolo:
O craqueamento é uma reação química empregada industrialmente para a obtenção de moléculas mais leves a partir de moléculas mais pesadas. Considere a equação termoquímica abaixo, que representa o processo utilizado em uma unidade industrial para o craqueamento de hexano.
H3C − CH2 − CH2 − CH2 − CH2 − CH3 (g) ⇌ H3C − CH2 − CH2 − CH3(g) + H2C = CH2 (g) ∆H >0
Em um experimento para avaliar a eficiência desse processo, a reação química foi iniciada sob temperatura T1 e pressão P1 . Após seis horas, a temperatura foi elevada para T2 , mantendo-se a pressão em P1 . Finalmente, após doze horas, a pressão foi elevada para P2 , e a temperatura foi mantida em T2 .
A variação da concentração de hexano no meio reacional ao longo do experimento está
representada em: