Questões de Vestibular
Foram encontradas 1.865 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
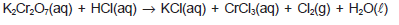
O dicromato de potássio reage com ácido clorídrico, de acordo com a equação química não balanceada apresentada.
Em relação a essa equação química e aos conhecimentos sobre classificação periódica, funções inorgânicas e reações químicas, pode-se afirmar:
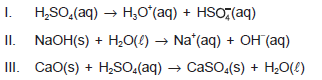
Com base nessas informações e nos conhecimentos sobre funções inorgânicas, reações químicas e soluções, pode-se afirmar:
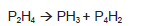
A equação química, não balanceada, representa um processo de obtenção da fosfina, PH3, um gás incolor cujo odor é semelhante ao de peixes em decomposição.
Balanceando-se essa equação, com os menores coeficientes inteiros e considerando-se os conhecimentos sobre ligações químicas, fórmulas químicas, reações químicas, é correto afirmar:
BICARBONATO DE SÓDIO PARA
COMBATER RESFRIADOS E GRIPES
Pode ajudar a manter um correto equilíbrio no pH do sangue, o que ajuda a combater e evitar as gripes e resfriados. Em 1924, o Dr. Volney S. Cheney, um médico que trabalhou para o serviço de saúde pública nos Estados Unidos, publicou o artigo “Arm & Hammer Baking Soda Medical Use” no qual relatou os resultados de alguns testes usando o bicarbonato de sódio, e o resultado foi que quem fez o tratamento com esse mágico mineral não contraiu nenhum resfriado ou gripe. O tratamento para resfriados, usando bicarbonato de sódio, é muito fácil de fazer, junte 1/2 colher de chá (0,03 mol) de bicarbonato de sódio em um copo de água fria (100 mL) e beba em seguida. Deve-se beber um copo de manhã e outro à noite até os sintomas do resfriado desaparecerem por completo.
Disponível em: http://www.remedios-caseiros.com/remedios/bicarbonatode-sodio.html. Adaptada. Acesso em: 11 de agosto de 2015.
[Dados: Kw = 1 · 10–14; Ka(H2CO3) = 4,3 · 10–7; √69 ≅ 8,3; 3/4,3 ≅ 0,69; log 8,3 ≅ 0,92]
De acordo com o texto, é pertinente inferir que o pH da solução de bicarbonato de sódio é, aproximadamente,
OS RISCOS DA FEBRE ALTA
Nós, como todos os mamíferos, somos animais homeotérmicos, isto é, nossa temperatura se mantém constante independentemente da temperatura do local onde nos encontramos. Todas as reações do complexo bioquímico representado por nosso organismo, como as envolvidas na digestão, ocorrem nessa temperatura. Quando temos febre, todas essas reações passam a ter sua velocidade aumentada. Uma elevação em 1 °C ou 2 °C na temperatura faz que elas se acelerem substancialmente. Como a temperatura corporal aumenta, o metabolismo se acelera, produzindo mais calor. Nesse processo, nosso ritmo respiratório aumenta porque a demanda de oxigênio passa a ser maior. Com isso, perdemos mais água, comprometendo o sistema circulatório, o que torna mais difícil a eliminação de calor pela pele. Acima de 41,5 °C, as funções celulares ficam muito prejudicadas, e o indivíduo perde a consciência, por isso febres altas podem ser fatais.
Disponível em: Química: ações e aplicações: 2ª série/Vera Lúcia Duarte de
Novais – 1ª ed. – São Paulo: FTD, 2013. Adaptado.
A análise do texto permite inferir que o risco de morte