Questões de Vestibular
Foram encontradas 637 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
O mineral calcita, CaCO3, é um dos principais constituintes do mármore. Esse mineral pode ser dissolvido com ácidos, porque ocorre a seguinte reação:
CaCO3 (s) + 2H+ (aq) → Ca2+ (aq) + CO2 (g) + H2O (l)
Considerando uma solução de ácido clorídrico cujo pH = 0, o volume dessa solução, em mL, necessário para dissolver 1,0 g de CaCO3 é deMassa molar do CaCO3 = 100 g.mol−1
Considere um corpo sólido de volume V. Ao flutuar em água, o volume de sua parte submersa é igual a V/8 ; quando colocado em óleo, esse volume passa a valer V/6.
Com base nessas informações, conclui-se que a razão entre a densidade do óleo e a da água corresponde a:
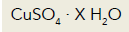
Uma amostra de 4,99 g desse sal hidratado foi aquecida até que toda a água nela contida evaporou, obtendo-se uma massa de 3,19 g de sulfato de cobre II. O número de mols de água por mol de sulfato de cobre II na composição do sal hidratado equivale a:
Utilize as informações a seguir para responder à questão.

A massa de cloreto de sódio a ser adicionada, em quilogramas, é igual a: