Questões de Vestibular Comentadas por alunos sobre transformações químicas em química
Foram encontradas 613 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Com as informações que podem ser obtidas da tabela periódica, relacione os elementos apresentados na coluna da esquerda com a informação da coluna à direita que indica a respectiva distribuição dos elétrons nos subníveis do último nível de energia ocupado no estado fundamental.
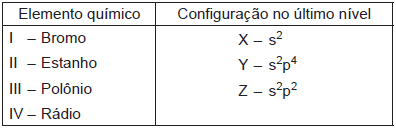
Estão corretas as associações:
NH4 NO3 → N2 (g) + 2 H2 O(g) + ½ O2 (g)
(Explosivos em Expansão, em Posto de Escuta: crônicas químicas e econômicas. Albert Hahn, Editora Cla, 2012. Adaptado)
Considerando um cartucho com a capacidade de 1,0 L, contendo 160 g de nitrato de amônio, no instante da ignição, quando ocorre a completa reação de decomposição do sal a 167 oC, a pressão no interior do cartucho, no instante de sua ruptura e explosão é, em atm, igual a aproximadamente
(Dado: R = 0,082 atm.L.mol–1 .K–1 )
Para representarem corretamente o modelo da molécula do C4H8O2, as bolas de plástico tinham tamanhos diferentes (pequenas, médias e grandes). Suas massas, em gramas, eram iguais aos valores das massas molares dos elementos C, H e O. Em escala ampliada para centímetros, seus raios tinham a mesma ordem de tamanho dos raios atômicos dos átomos que representavam.
Sobre essas bolas de plástico que representam as características de tamanho e massa dos átomos de C, H e O, os alunos concluíram:
I. as bolas que representam os átomos de H eram as pequenas, e as que representam os átomos de O eram as grandes;
II. a massa total das bolas grandes correspondia a seis vezes a massa total das bolas de tamanho pequeno;
III. a massa total das bolas pequenas correspondia a ¼ da massa total das bolas de tamanho médio.
Classificando cada uma das conclusões como verdadeira (V) ou falsa (F), tem-se, correta e respectivamente:
Considere: R = 0,082 atm L mol-1 K-1
M(O2) = 32 g mol-1