Questões de Vestibular Sobre termoquímica: energia calorífica, calor de reação, entalpia, equações e lei de hess. em química
Foram encontradas 341 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
A equação química que representa a reação que ocorre na fermentação alcoólica da glicose é
C6H12O6(aq) → 2 C2H6O(aq) + 2 CO2(g) ΔrH = ?
Assinale a alternativa que apresenta o valor correto da entalpia padrão da reação (ΔrH) de fermentação da glicose, em kJ/mol.
Entalpias de formação em kJ/mol
Substância ΔfH C6H12O6(aq) – 1 277 C2H6O (aq) – 278 CO2(g) – 394
O poder calorífico de um gás liquefeito é conhecido como a quantidade de energia liberada pela sua queima. Se o poder calorífico do propano é cerca de 50 kJ/g, assinale a alternativa que apresenta, corretamente, o volume, em m3 , de propano que deve ser queimado para liberar 1,0×103 kJ de energia, à temperatura de 20 ◦C e 1 atmosfera.
Dados: Massa molar do propano = 44,1 g/mol
Pode-se concluir corretamente que, na combustão completa de 1 mol desse hidrocarboneto, as quantidades de matéria, e CO2 e de H2O produzidas são, em mol, respectivamente, iguais a
Entre os gráficos 1, 2 e 3, aquele que representa corretamente a reação da fosfina com o oxigênio, descrita no texto, é o
Leia o texto para responder a questão.
De onde vem o cheiro de carro novo?
De acordo com o gerente de uma montadora de veículos, o cheiro é composto por uma combinação de vários tipos de substâncias químicas usadas na fabricação do veículo, incluindo solventes, plásticos, colas, tecidos e borracha. Porém, muitas delas são altamente tóxicas, porque contêm Compostos Orgânicos Voláteis (COVs) em sua composição, como benzeno, tolueno e formol, que podem ser letais dependendo da quantidade. Eles acabam escapando e impregnando o ar, porque não requerem altas temperaturas para evaporarem.
<http://tinyurl.com/y8ucob6c> Acesso em: 13.11.2017. Adaptado.
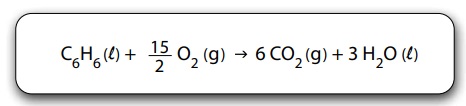
A entalpia de combustão do benzeno pode ser determinada conhecendo-se os valores das entalpias de formação do gás carbônico, assim como da água e do benzeno líquidos.
A tabela apresenta os valores de entalpia de formação de algumas substâncias nas condições padrão.
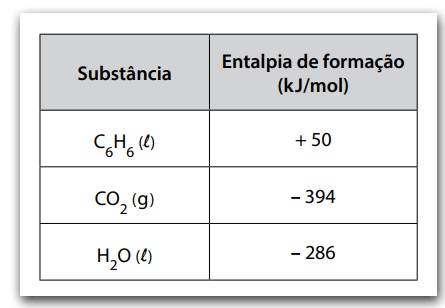
A entalpia de combustão completa do benzeno, em kJ/mol, é