Questões de Vestibular Sobre termoquímica: energia calorífica, calor de reação, entalpia, equações e lei de hess. em química
Foram encontradas 341 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
INSTRUÇÃO: Para responder à questão, analise
as informações a seguir.
O fogo sempre foi objeto de fascínio e instrumento de extrema utilidade para o ser humano. Mesmo hoje, com o uso cada vez mais disseminado da energia elétrica, não deixamos de utilizar o fogo no cotidiano: ainda queimamos carvão na churrasqueira, lenha na lareira, gás liquefeito de petróleo no fogão e parafina nas velas.
Sobre esse assunto, são apresentadas as seguintes afirmativas:
I. A combustão é uma reação redox em que o comburente age como oxidante.
II. Na combustão do gás de cozinha, há produção de água, mas na do carbono não há.
III. A velocidade de combustão do carvão em pedaços é igual à do carvão em pó.
IV. As reações de combustão são exotérmicas e liberam gás carbônico.
Em relação à combustão, são corretas somente as
afirmativas
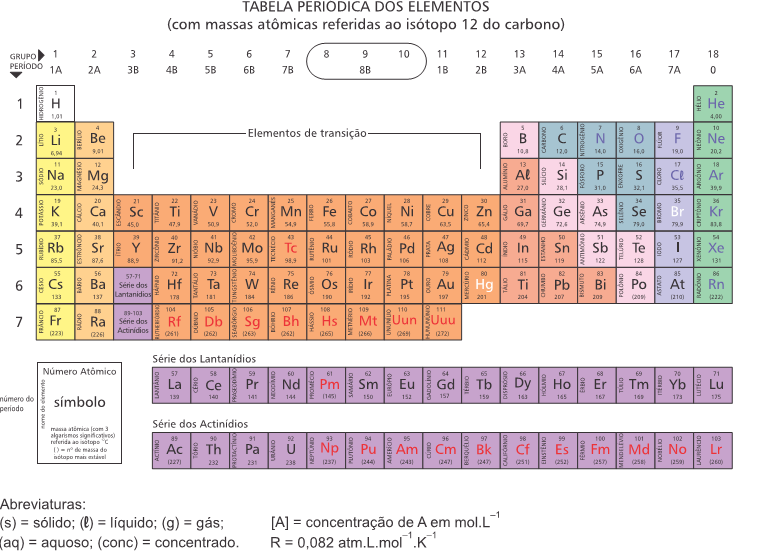
Dados:
Entalpia de formação padrão do O3 : 143 kJ.mol–1
Entalpia de ligação O=O: 498 kJ.mol-1
NO (g) + O3(g) → NO2(g) + O2(g) ΔHθ = – 200 kJ
Diversas reações ocorrem na atmosfera devido à ação da luz solar e à presença de poluentes. Uma das reações relevantes é a decomposição do dióxido de nitrogênio em óxido nítrico e oxigênio atômico.
NO2(g) → NO(g) + O(g)
A partir dos dados é possível concluir que essa reação é
O ácido nítrico é um importante insumo para produção de fertilizantes, explosivos e tintas. Sua produção industrial é feita pelo processo Ostwald, em três etapas que podem ser representadas pelas reações:
I. 6 NH3 (g) + 15/2 O2 (g) → 6 NO (g) + 9 H2O (g) ∆H = – 1378 kJ
II. 6 NO (g) + 3 O2 (g) → 6 NO2 (g) ∆H = – 339 kJ
III. 6 NO2
(g) + 2 H2O (g) → 4 HNO3
(aq) + 2 NO (g) ∆H = – 270 kJ
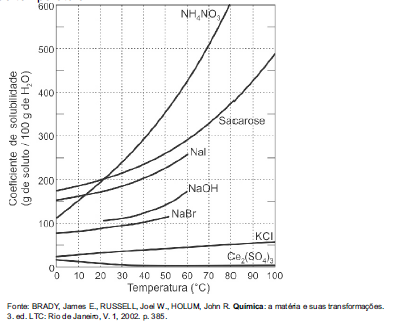
Considerando as informações apresentadas pelo gráfico acima, assinale a alternativa correta.