Questões ENEM de Química
Foram encontradas 454 questões
A obtenção de energia por meio da fissão nuclear do 235U é muito superior quando comparada à combustão da gasolina. O calor liberado na fissão do 235U é 8 x 1010 J/g e na combustão da gasolina é 5 x 104 J/g.
A massa de gasolina necessária para obter a mesma energia na fissão de 1 kg de 235U é da ordem de
Um produtor rural registrou queda de produtividade numa das áreas de plantio de arroz de sua propriedade. Análises químicas revelaram concentrações elevadas do íon amónio (NH4+) e baixas dos íons nitrito (NO2-) e nitrato (NO3-) no solo. Esses compostos nitrogenados são necessários para o crescimento dos vegetais e participam do ciclo biogeoquímico do nitrogênio.
Em qual etapa desse ciclo biogeoquímico são formados os compostos que estão em baixa concentração nesse solo?
O descarte do óleo de cozinha na rede de esgotos gera diversos problemas ambientais. Pode-se destacar a contaminação dos cursos-d’água, que tem como uma das consequências a formação de uma película de óleo na superfície, causando danos à fauna aquática, por dificultar as trocas gasosas, além de diminuir a penetração dos raios solares no curso hídrico.
Disponível em: http://revistagalileu.globo.com. Acesso em: 3 ago. 2012 (adaptado).
Qual das propriedades dos óleos vegetais está relacionada aos problemas ambientais citados?
As emissões de dióxido de carbono (CO2) por veículos são dependentes da constituição de cada tipo de combustível. Sabe-se que é possível determinar a quantidade emitida de CO2, a partir das massas molares do carbono e do oxigênio, iguais a 12 g/mol e 16 g/mol, respectivamente. Em uma viagem de férias, um indivíduo percorreu 600 km em um veículo que consome um litro de gasolina a cada 15km de percurso.
Considerando que o conteúdo de carbono em um litro dessa gasolina é igual a 0,6 kg, a massa de CO2 emitida pelo veículo no ambiente, durante a viagem de férias descrita, é igual a
O processo de dessulfurização é uma das etapas utilizadas na produção do diesel. Esse processo consiste na oxidação do enxofre presente na forma de sulfeto de hidrogênio (H2S) a enxofre elementar (sólido) que é posteriormente removido. Um método para essa extração química é o processo Claus, no qual parte do H2S é oxidada a dióxido de enxofre (SO2) e, então, esse gás é usado para oxidar o restante do H2S. Os compostos de enxofre remanescentes e as demais moléculas presentes no diesel sofrerão combustão no motor.
MARQUES FILHO, J. Estudo da fase térmica do processo Claus utilizando fluidodinâmica computacional. São Paulo: USP, 2004 (adaptado).
O benefício do processo Claus é que, na combustão do diesel, é minimizada a emissão de gases
Combustíveis automotivos têm sido adulterados pela adição de substâncias ou materiais de baixo valor comercial. Esse tipo de contravenção pode danificar os motores, aumentar o consumo de combustível e prejudicar o meio ambiente. Vários testes laboratoriais podem ser utilizados para identificar se um combustível está ou não adulterado. A legislação brasileira estabelece que o diesel, obtido do petróleo, contenha certa quantidade de biodiesel. O quadro apresenta valores de quatro propriedades do diesel, do biodiesel e do óleo vegetal, um material comumente utilizado como adulterante.
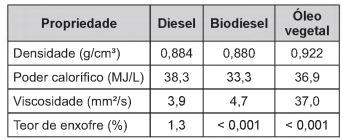
Com base nas informações apresentadas no quadro, quais
são as duas propriedades que podem ser empregadas
tecnicamente para verificar se uma amostra de diesel
comercial está ou não adulterada com óleo vegetal?
As águas dos oceanos apresentam uma alta concentração de íons e pH entre 8,0 e 8,3. Dentre esses íons estão em equilíbrio as espécies carbonato (CO32-) e bicarbonato (HCO3-), representado pela equação química:
HCO3-(aq) ⇌ CO32-(aq) + H+(aq)
As águas dos rios, ao contrário, apresentam concentrações muito baixas de íons e substâncias básicas, com um pH em torno de 6. A alteração significativa do pH das águas dos rios e oceanos pode mudar suas composições químicas, por precipitação de espécies dissolvidas ou redissolução de espécies presentes nos sólidos suspensos ou nos sedimentos.
A composição dos oceanos é menos afetada pelo lançamento de efluentes ácidos, pois os oceanos
A busca por substâncias capazes de minimizar a ação do inseto que ataca as plantações de tomate no Brasil levou à síntese e ao emprego de um feromônio sexual com a seguinte fórmula estrutural:

Uma indústria agroquímica necessita sintetizar um derivado com maior eficácia. Para tanto, o potencial substituto deverá preservar as seguintes propriedades estruturais do feromônio sexual: função orgânica, cadeia normal e a isomeria geométrica original.
A fórmula estrutural do substituto adequado ao feromônio sexual obtido industrialmente é:
A água consumida na maioria das cidades brasileiras é obtida pelo tratamento da água de mananciais. A parte inicial do tratamento consiste no peneiramento e sedimentação de partículas maiores. Na etapa seguinte, dissolvem-se na água carbonato de sódio e, em seguida, sulfato de alumínio. O resultado é a precipitação de hidróxido de alumínio, que é pouco solúvel em água, o qual leva consigo as partículas poluentes menores. Posteriormente, a água passa por um processo de desinfecção e, finalmente, é disponibilizada para o consumo.
No processo descrito, a precipitação de hidróxido de alumínio é viabilizada porque
Para comparar a eficiência de diferentes combustíveis, costuma-se determinar a quantidade de calor liberada na combustão por mol ou grama de combustível. O quadro mostra o valor de energia liberada na combustão completa de alguns combustíveis.
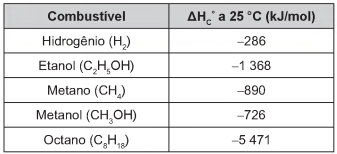
As massas molares dos elementos H, C e O são iguais a 1 g/mol, 12 g/mol e 16 g/mol, respectivamente.
ATKINS, P Princípios de química. Porto Alegre: Bookman, 2007 (adaptado).
Qual combustível apresenta maior liberação de energia
por grama?
Atualmente, soldados em campo, seja em treinamento ou em combate, podem aquecer suas refeições, prontas e embaladas em bolsas plásticas, utilizando aquecedores químicos, sem precisar fazer fogo. Dentro dessas bolsas existe magnésio metálico em pó e, quando o soldado quer aquecer a comida, ele coloca água dentro da bolsa, promovendo a reação descrita pela equação química:
Mg (s) + 2 H2O (I) → Mg(OH)2 (s) + H2 (g) + 350 kJ
O aquecimento dentro da bolsa ocorre por causa da
Climatério é o nome de um estágio no processo de amadurecimento de determinados frutos, caracterizado pelo aumento do nível da respiração celular e do gás etileno (C2H4). Como consequência, há o escurecimento do fruto, o que representa a perda de muitas toneladas de alimentos a cada ano.
É possível prolongar a vida de um fruto climatérico pela eliminação do etileno produzido. Na indústria, utiliza-se o permanganato de potássio (KMnO4) para oxidar o etileno a etilenoglicol (HOCH2CH2OH), sendo o processo representado de forma simplificada na equação:
2KMnO4+3 C2H4+4H2O → 2 MnO2 + 3HOCH2CH2OH + 2KOH
O processo de amadurecimento começa quando a concentração de etileno no ar está em cerca de 1,0 mg de C2H4 por kg de ar.
As massas molares dos elementos H, C, O, K e Mn são, respectivamente, iguais a 1 g/mol, 12g/mol, 16g/mol, 39 g/mol e 55 g/mol.
A fim de diminuir essas perdas, sem desperdício de
reagentes, a massa mínima de KMnO4 por kg de ar é mais
próxima de
Um bafômetro simples consiste em um tubo contendo uma mistura sólida de dicromato de potássio em sílica umedecida com ácido sulfúrico. Nesse teste, a detecção da embriaguez por consumo de álcool se dá visualmente, pois a reação que ocorre é a oxidação do álcool a aldeído e a redução do dicromato (alaranjado) a cromo(lll) (verde) ou cromo(ll) (azul).
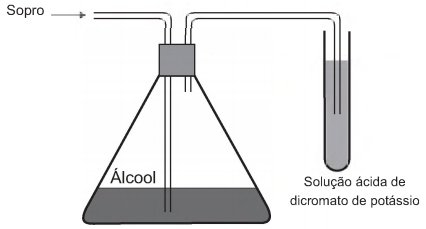
A equação balanceada da reação química que representa esse teste é:
A crescente produção industrial lança ao ar diversas substâncias tóxicas que podem ser removidas pela passagem do ar contaminado em tanques para filtração por materiais porosos, ou para dissolução em água ou solventes orgânicos de baixa polaridade, ou para neutralização em soluções ácidas ou básicas. Um dos poluentes mais tóxicos liberados na atmosfera pela atividade industrial é a 2,3,7,8-tetraclorodioxina.
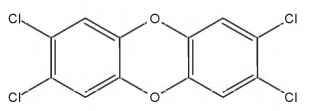
Esse poluente pode ser removido do ar pela passagem através de tanques contendo
Adicionar quantidades de álcool à gasolina, diferentes daquelas determinadas pela legislação, é uma das formas de adulterá-la. Um teste simples para aferir a quantidade de álcool presente na mistura consiste em adicionar uma solução salina aquosa à amostra de gasolina sob análise.
Essa metodologia de análise pode ser usada porque o(a)
O quadro apresenta alguns exemplos de combustíveis empregados em residências, indústrias e meios de transporte.
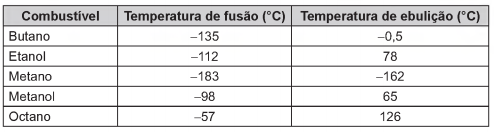
São combustíveis líquidos à temperatura ambiente de 25 ºC:
A absorção e o transporte de substâncias tóxicas em sistemas vivos dependem da facilidade com que estas se difundem através das membranas das células. Por apresentar propriedades químicas similares, testes laboratoriais empregam o octan-1-ol como modelo da atividade das membranas. A substância a ser testada é adicionada a uma mistura bifásica do octan-1-ol com água, que é agitada e, ao final, é medido o coeficiente de partição octan-1-ol:água (Koa):
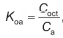
em que Coct é a concentração da substância na fase do octan-1-ol, e Ca a concentração da substância na fase aquosa.
Foram avaliados cinco poluentes de sistemas aquáticos: benzeno, butano, éter dietílico, fluorobutano e metanol.
O poluente que apresentou Koa tendendo a zero é o
A horticultura tem sido recomendada para a agricultura familiar, porém as perdas são grandes devido à escassez de processos compatíveis para conservar frutas e hortaliças. O processo, denominado desidratação osmótica, tem se mostrado uma alternativa importante nesse sentido, pois origina produtos com boas condições de armazenamento e qualidade semelhante à matéria-prima.
GOMES, A. T.; CEREDA, M. P.; VILPOUX, O. Desidratação osmótica: uma tecnologia de baixo custo para o desenvolvimento da agricultura familiar. Revista Brasileira de Gestão e Desenvolvimento Regional, n. 3, set.-dez. 2007 (adaptado).
Esse processo para conservar os alimentos remove a água por
No Brasil, os postos de combustíveis comercializavam uma gasolina com cerca de 22% de álcool anidro. Na queima de 1 litro desse combustível são liberados cerca de 2 kg de CO2 na atmosfera. O plantio de árvores pode atenuar os efeitos dessa emissão de CO2. A quantidade de carbono fixada por uma árvore corresponde a aproximadamente 50% de sua biomassa seca, e para cada 12 g de carbono fixados, 44 g de CO2 são retirados da atmosfera. No Brasil, o plantio de eucalipto (Eucalyptus grandis) é bem difundido, sendo que após 11 anos essa árvore pode ter a massa de 106 kg, dos quais 29 kg são água.
Uma única árvore de Eucalyptus grandis, com as características descritas, é capaz de fixar a quantidade de CO2 liberada na queima de um volume dessa gasolina mais próximo de
O hidrocarboneto representado pela estrutura química a seguir pode ser isolado a partir das folhas ou das flores de determinadas plantas. Além disso, sua função é relacionada, entre outros fatores, a seu perfil de insaturações.
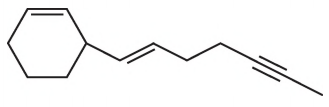
Considerando esse perfil específico, quantas ligações pi
a molécula contém?