Questões do Enem Comentadas sobre química
Foram encontradas 459 questões
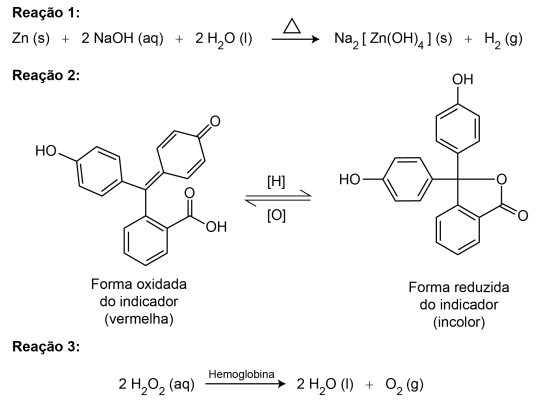
DIAS FILHO, C. R.; ANTEDOMENICO, E. A perícia criminal e a interdisciplinaridade no ensino de ciências naturais. Química Nova na Escola, n. 2, maio 2010 (adaptado).
A mudança de coloração que indica a presença de sangue ocorre por causa da reação do indicador com o(a)
A diferença de emissão de CO2 dos carros desse fabricante em relação ao limite estabelecido na União Europeia é
As populares pilhas zinco-carbono (alcalinas e de Leclanché) são compostas por um invólucro externo de aço (liga de ferro-carbono), um ânodo (zinco metálico), um cátodo (grafita) e um eletrólito (MnO2 mais NH4Cl ou KOH), contido em uma massa úmida com carbono chamada pasta eletrolítica. Os processos de reciclagem, geralmente propostos para essas pilhas usadas, têm como ponto de partida a moagem (trituração). Na sequência, uma das etapas é a separação do aço, presente no invólucro externo, dos demais componentes.
Que processo aplicado à pilha moída permite obter essa separação?
Os objetos de prata tendem a escurecer com o tempo, em contato com compostos de enxofre, por causa da formação de uma película superficial de sulfeto de prata (Ag2S), que é escuro. Um método muito simples para restaurar a superfície original desses objetos é mergulhá-los em uma solução diluída aquecida de hidróxido de sódio (NaOH), contida em uma panela comum de alumínio. A equação química que ilustra esse processo é:
3 Ag2S (s) + 2 Al (s) + 8 NaOH (aq) → 6 Ag (s) + 3 Na2S (aq) + 2 NaAlO2 (aq) + 4 H2O (l)
A restauração do objeto de prata ocorre por causa do(a)
As pilhas recarregáveis, bastante utilizadas atualmente, são formadas por sistemas queatuam como uma célula galvânica, enquanto estão sendo descarregadas, e como célulaeletrolítica, quando estão sendo recarregadas.
Uma pilha é formada pelos elementos níquel e cádmio e seu carregador deve forneceruma diferença de potencial mínima para promover a recarga. Quanto maior a diferença depotencial gerada pelo carregador, maior será o seu custo. Considere os valores de potencialpadrão de redução dessas espécies:
Ni2+ (aq) + 2 e− ⇌ Ni (s) E° = −0,230 V
Cd2+ (aq) + 2 e− ⇌ Cd (s) E° = −0,402 V
Teoricamente, para que um carregador seja ao mesmo tempo eficiente e tenha o menor preço,
a diferença de potencial mínima, em volt, que ele deve superar é de
Qual é o processo envolvido na detonação dessa bomba?
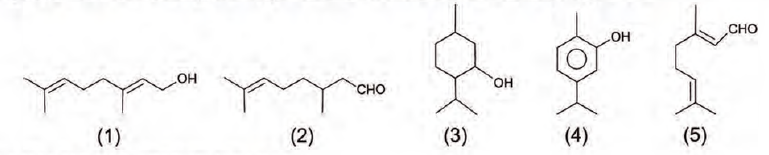
Qual substância o empresário deverá utilizar?
BRUNNING, A. The Chemistry of Firework Pollution. Disponível em: www.compoundchem.com. Acesso em: 1 dez. 2017 (adaptado).
Esses espetáculos promovem riscos ambientais, porque
Esses polímeros têm grandes vantagens socioambientais em relação aos convencionais porque
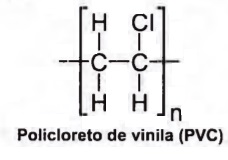
Para realizar esse experimento, o estudante colocou uma amostra de filme de PVC em um tubo de ensaio e o aqueceu, promovendo a decomposição térmica. Houve a liberação majoritária de um gás diatômico heteronuclear que foi recolhido em um recipiente acoplado ao tubo de ensaio. Esse gás, quando borbulhado em solução alcalina diluída contendo indicador ácido-base, alterou a cor da solução. Além disso, em contato com uma solução aquosa de carbonato de sódio (Na2CO3), liberou gás carbônico.
Qual foi o gás liberado majoritariamente na decomposição térmica desse tipo de plástico?
A obtenção de óleos vegetais, de maneira geral, passa pelas etapas descritas no quadro.
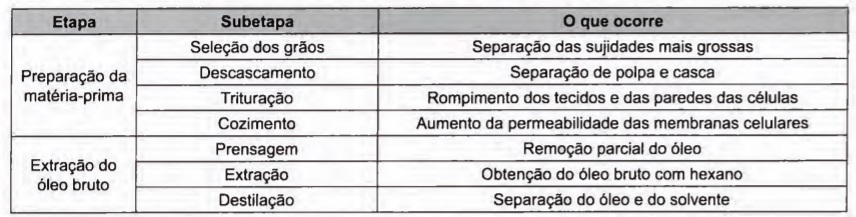
Qual das subetapas do processo é realizada em função apenas da polaridade das substâncias?
Para garantir que produtos eletrônicos estejam armazenados de forma adequada antes da venda, algumas empresas utilizam cartões indicadores de umidade nas embalagens desses produtos. Alguns desses cartões contêm um sal de cobalto que muda de cor em presença de água, de acordo com a equação química:
CoCI2(s) + 6 H2O (g) ⇌ CoCI2 • 6H2O (s) ΔH<0
(azul) (rosa)
Como você procederia para reutilizar, num curto intervalo de tempo, um cartão que já estivesse com a coloração rosa?
O êxito da aplicação dessa tecnologia é por causa da realização de reações químicas que ocorrem em condições de
Os impactos decorrentes desse derramamento ocorrem porque os componentes do petróleo
Considere os dados do acetato de etila: • Baixa solubilidade em água; • Massa específica = 0,9 g cm-3; • Temperatura de fusão = - 83 °C; • Pressão de vapor maior que a da água.
A fim de tratar o resíduo, recuperando o acetato de etila, o técnico deve
C2H5OH (I) + 3 O2 (g) → 2 CO2 (g) + 3 H2O (g)
Foram analisadas as emissões de CO2 envolvidas em dois veículos, um movido a etanol e outro elétrico, em um mesmo trajeto de 1.000 km.
CHIARADIA, C. A. Estudo da viabilidade da implantação de frotas de veículos elétricos e híbridos elétricos no atual cenário econômico, político, energético e ambiental brasileiro. Guaratinguetá: Unesp. 2015 (adaptado).
A quantidade equivalente de etanol economizada, em quilograma, com o uso do veículo elétrico nesse trajeto, é mais próxima de
Qual é a concentração de sacarose depois de 400 minutos do início da reação de hidrólise?
A causa principal desse risco era o(a)
Que volume de larvicida deve conter o frasco plástico?
Os compostos contidos no calcário dolomítico elevam o pH do solo, pois