Questões do Enem
Sobre substâncias e suas propriedades em química
Foram encontradas 60 questões
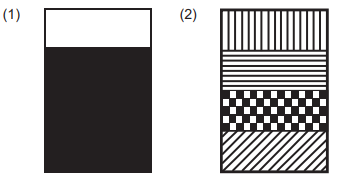
Na lavagem a seco, um solvente é considerado efetivo para limpeza de roupas quando evita o encolhimento dos tecidos, evapora facilmente e dissolve manchas lipofílicas, como óleos, ceras e gorduras em geral, por apresentar polaridade similar.
BORGES, L.; MACHADO, P. F. L. Lavagem a seco. Química Nova na Escola, n. 1, fev. 2013.
Qual estrutura molecular representa o solvente mais efetivo na lavagem a seco de roupas?
As propriedades de líquidos e soluções que justificam os resultados obtidos nos experimentos 1 e 2 são
bula de um determinado medicamento traz as seguintes informações:

De acordo com as informações apresentadas na bula,
a substância que se encontra em maior concentração
e a não condutora de corrente elétrica, quando em
solução aquosa, são, respectivamente,
24 Ag (s) + 8 Sn (s) + 37 Hg (l) → 12 Ag2 Hg3 (s) + Sn8 Hg (s)
Os materiais formados pelos elementos citados são caracterizados como
Hg2(NO3 )2 (aq) + 2 NaCl (aq) ➝ Hg2Cl2 (s) + 2 NaNO3 (aq)
Na dúvida sobre a massa de NaCl a ser utilizada, o assistente aumentou gradativamente a quantidade adicionada em cada frasco, como apresentado no quadro.
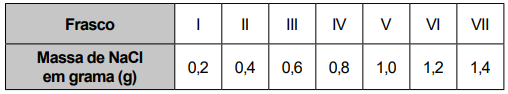
O produto obtido em cada experimento foi filtrado, secado e teve sua massa aferida. O assistente organizou os resultados na forma de um gráfico que correlaciona a massa de NaCl adicionada com a massa de Hg2Cl2 obtida em cada frasco. A massa molar do Hg2 (NO3 )2 é 525 g mol–1, a do NaCl é 58 g mol–1 e a do Hg2Cl2 é 472 g mol–1.
Qual foi o gráfico obtido pelo assistente de laboratório?
Atualização da recomendação da Sociedade Portuguesa de Neonatologia. Disponível em: www.spneonatologia.pt. Acesso em: 22 out. 2021 (adaptado).
Caso esse suplemento seja acondicionado em embalagem desse tipo de vidro, o risco de contaminação por alumínio será maior se o(a)
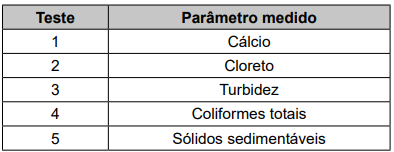
Qual teste deve ser considerado para controlar a formação desse tipo de obstrução de tubulações?
A água bruta coletada de mananciais apresenta alto índice de sólidos suspensos, o que a deixa com um aspecto turvo. Para se obter uma água límpida e potável, ela deve passar por um processo de purificação numa estação de tratamento de água. Nesse processo, as principais etapas são, nesta ordem: coagulação, decantação, filtração, desinfecção e fluoretação.
Qual é a etapa de retirada de grande parte desses sólidos?

A figura é uma representação esquemática de uma estação de tratamento de água. Nela podem ser observadas as etapas que vão desde a captação em represas até a distribuição à população. No intuito de minimizar o custo com o tratamento, foi proposta a eliminação da etapa de adição de hipoclorito de sódio e o resultado foi comparado com o da água tratada em todas as etapas.
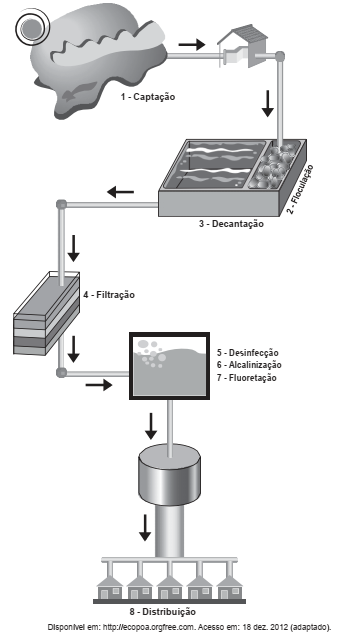
Caso fosse aceita a proposta apresentada, qual seria a
mudança principal observada na qualidade da água que
seria distribuída às residências?
Para preparar o vinho de laranja, caldo de açúcar é misturado com suco de laranja, e a mistura é passada em panos para retenção das impurezas. O líquido resultante é armazenado em garrafões, que são tampados com rolhas de cortiça. Após oito dias de repouso, as rolhas são substituídas por cilindros de bambu e, finalmente, após dois meses em repouso ocorre novamente a troca dos cilindros de bambu pelas rolhas de cortiça.
RESENDE, D. R.; CASTRO, R. A.; PINHEIRO, P. C. O saber popular nas aulas de química: relato de experiência envolvendo a produção do vinho de laranja e sua interpretação no ensino médio. Química Nova na Escola, n. 3, ago. 2010 (adaptado).
Os processos físico e químico que ocorrem na fabricação dessa bebida são, respectivamente,
Os compostos iônicos CaCO3 e NaCl têm solubilidades muito diferentes em água. Enquanto o carbonato de cálcio, principal constituinte do mármore, é praticamente insolúvel em água, o sal de cozinha é muito solúvel. A solubilidade de qualquer sal é o resultado do balanço entre a energia de rede (energia necessária para separar completamente os íons do sólido cristalino) e a energia envolvida na hidratação dos íons dispersos em solução.
Em relação à energia de rede, a menor solubilidade do primeiro composto é explicada pelo fato de ele apresentar maior
A densidade é uma propriedade que relaciona massa e volume de um material. Um estudante iniciou um procedimento de determinação da densidade de uma amostra sólida desconhecida. Primeiro ele determinou a massa da amostra, obtendo 27,8 g. Em seguida, utilizou uma proveta, graduada em mililitro, com água para determinar o volume da amostra, conforme esquematizado na figura. Considere a densidade da água igual a 1 g/mL.
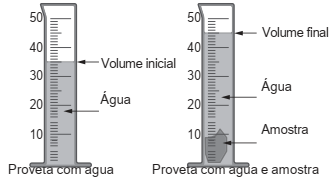
A densidade da amostra obtida, em g/mL, é mais
próxima de
Para demonstrar os processos físicos de separação de componentes em misturas complexas, um professor de química apresentou para seus alunos uma mistura de limalha de ferro, areia, cloreto de sódio, bolinhas de isopor e grãos de feijão. Os componentes foram separados em etapas, na seguinte ordem:
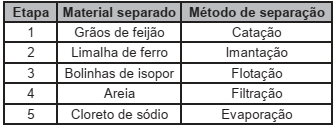
Em qual etapa foi necessário adicionar água para dar
sequência às separações?
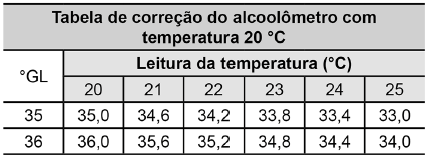 Manual alcoolômetro Gay Lussac. Disponível em: www.incoterm.com.br.
Acesso em: 4 dez. 2018 (adaptado).
Manual alcoolômetro Gay Lussac. Disponível em: www.incoterm.com.br.
Acesso em: 4 dez. 2018 (adaptado).
É necessária a correção da medida do instrumento, pois um aumento na temperatura promove o(a)
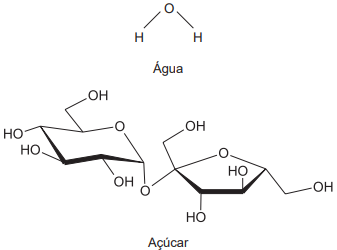
A dissolução na água, do soluto apresentado, ocorre predominantemente por meio da formação de
Para assegurar a boa qualidade de seu produto, uma indústria de vidro analisou um lote de óxido de silício (SiO2), principal componente do vidro. Para isso, submeteu uma amostra desse óxido ao aquecimento até sua completa fusão e ebulição, obtendo ao final um gráfico de temperatura T (°C) versus tempo t (min). Após a obtenção do gráfico, o analista concluiu que a amostra encontrava-se pura.
Dados do SiO2: Tfusão = 1 600 °C; Tebulição = 2 230 °C.
Qual foi o gráfico obtido pelo analista?
Entre os materiais mais usados no nosso dia a dia destacam-se os plásticos, constituídos por polímeros. A consequência de seu amplo uso é a geração de resíduos, que necessitam de um destino final adequado em termos ambientais. Uma das alternativas tem sido a reciclagem, que deve respeitar as características dos polímeros que compõem o material. Esse processo envolve algumas etapas, como: separação do resíduo (catação), moagem, hidrólise, lavagem, secagem, pirólise e aquecimento (fusão).
SPINACÉ, M. A. S., PAOLI, M. A. D. Tecnologia de reciclagem de polímeros. Química Nova, n.1, 2005 (adaptado).
Quais das etapas citadas do processo de reciclagem são classificadas como métodos
químicos?
As populares pilhas zinco-carbono (alcalinas e de Leclanché) são compostas por um invólucro externo de aço (liga de ferro-carbono), um ânodo (zinco metálico), um cátodo (grafita) e um eletrólito (MnO2 mais NH4Cl ou KOH), contido em uma massa úmida com carbono chamada pasta eletrolítica. Os processos de reciclagem, geralmente propostos para essas pilhas usadas, têm como ponto de partida a moagem (trituração). Na sequência, uma das etapas é a separação do aço, presente no invólucro externo, dos demais componentes.
Que processo aplicado à pilha moída permite obter essa separação?
A obtenção de óleos vegetais, de maneira geral, passa pelas etapas descritas no quadro.
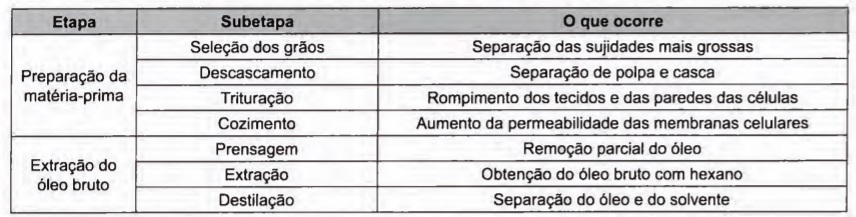
Qual das subetapas do processo é realizada em função apenas da polaridade das substâncias?