Questões Militares
Comentadas sobre física térmica - termologia em física
Foram encontradas 198 questões
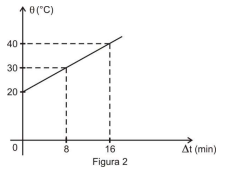
Com a temperatura θ lida no termômetro T, obteve-se, em função do tempo de aquecimento Δt, o gráfico representado na Figura 2.
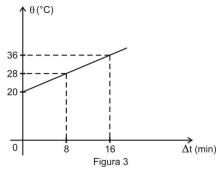
2ª etapa: repete-se a experiência, desde o início, desta vez, colocando o objeto de material desconhecido imerso na água. Sem alterar a quantidade de água, a corrente e a tensão no circuito elétrico, obteve-se o gráfico representado na Figura 3.
Considerando que, em ambas as etapas, toda energia elétrica foi dissipada por efeito Joule no resistor R, pode-se concluir que o calor específico do material de que é feito o objeto é, em cal/(g∙°C) igual a
Água (líquida) = 1 cal/gºC Alumínio (Al) = 0,22 cal/gºC Gelo = 0,50 cal/gºC Mercúrio (Hg) = 0,03 cal/gºC Areia = 0,12 cal/gºC Prata (Ag) = 0,05 cal/gºC Vidro = 0,20 cal/gºC Ferro (Fe) = 0,11 cal/gºC
Consultando a tabela, avalie as afirmativas a seguir.
I. A água, por ter um calor específico muito alto, é um excelente elemento termorregulador. A ausência de água faz com que, nos desertos, ocorram enormes diferenças entre a temperatura máxima e a mínima em um mesmo dia. II. Para refrigerar uma peça aquecida, é comum mergulhá-la em água. Será mais eficiente, para resfriá-la, mergulhá-la em mercúrio. Só não se faz isso porque, além de muito caro, seus vapores são extremamente tóxicos. III. Se cedermos a mesma quantidade de calor a amostras de massas iguais de alumínio e ferro, a temperatura da amostra de ferro aumentará o dobro do que aumenta a amostra de alumínio.
Está correto o que se afirma em
Texto 1A3-III
Muitos dos incêndios modernos ocorrem em ambientes fechados, condição que impõe uma dinâmica característica ao fogo e à sua propagação. No espaço confinado, observa-se o fenômeno do flashover, no qual ocorre uma ignição instantânea de materiais combustíveis voláteis que foram levados ao estado de combustão iminente pela temperatura ambiente, que gradativamente se eleva. O gráfico seguinte mostra a evolução da temperatura em relação ao tempo durante o início de um incêndio.

Texto 1A3-III
Muitos dos incêndios modernos ocorrem em ambientes fechados, condição que impõe uma dinâmica característica ao fogo e à sua propagação. No espaço confinado, observa-se o fenômeno do flashover, no qual ocorre uma ignição instantânea de materiais combustíveis voláteis que foram levados ao estado de combustão iminente pela temperatura ambiente, que gradativamente se eleva. O gráfico seguinte mostra a evolução da temperatura em relação ao tempo durante o início de um incêndio.

Dados: calor específico do alumínio = 0,2 cal/g ºC ; calor latente de fusão do aluminio= 94 cal/g
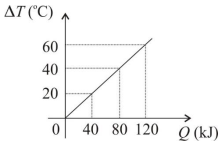
Um objeto de massa m = 500 g recebe uma certa quantidade de calor Q e, com isso, sofre uma variação de temperatura ΔT. A relação entre ΔT e Q está representada no gráfico ao lado.
Assinale a alternativa que apresenta corretamente o valor do calor específico c desse objeto.
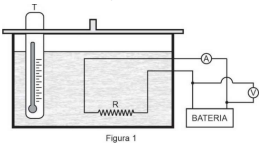
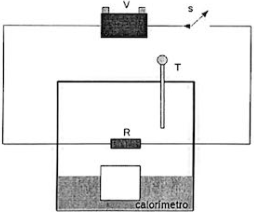
Um calorímetro está acoplado a um circuito elétrico composto por uma bateria que fornece uma tensão V = 10 V. uma chave S e um resistor de resistência R = 1,0 Ω capaz de fornecer energia térmica a seu interior. Um termômetro T também está no interior do calorímetro. conforme figura abaixo. Utilizando esse equipamento, foi feito o seguinte procedimento experimental:
1. colocou-se 100 g de água a 10 °C e 50 g de gelo com temperatura de - 10 °C no calorímetro;
2. ligou-se a chave S por 220 s e desligou-se em seguida;
3. esperou-se que o termômetro T indicasse que o sistema (água + gelo) alcançara o equilíbrio térmico e, então, foi feita a leitura da temperatura interna.
Considerando-se que o termômetro e o calorímetro têm capacidade térmica desprezível e toda energia dissipada pelo resistor se converteu em calor, espera-se que a temperatura indicada no termômetro T seja de:
(Dados: calor específico do gelo = 0,5 cal/g.°C; calor específico da água 1,0 cal/g.°C; calor latente de fusão do gelo = 80 cal/g; 1 cal = 4 J)
Nas questões de Física, quando necessário, use:
• massa atômica do hidrogênio: mH = 1,67⋅10 –27 kg
• massa atômica do hélio: mHe = 6,65⋅10 –27 kg
• velocidade da luz no vácuo: c = 3⋅10 8 m/s
• constante de Planck: h = 6⋅10 –34 J⋅s
• 1 eV = 1,6⋅10 –19 J
• constante eletrostática do vácuo: k0 = 9,0⋅10 9 N⋅m 2 / C2
• aceleração da gravidade: g = 10 m/s2
• cos 30º = sen 60º = √3/2
• cos 60º = sen 30º = √1/2
• cos 45º = sen 45º = √2/2
Considere uma dada massa gasosa de um gás perfeito que pode ser submetida a três transformações cíclicas diferentes I, II e III, como mostram os respectivos diagramas abaixo.
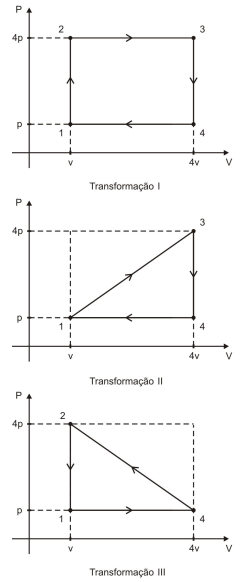
O gás realiza trabalhos totais τI, τII e τIII respectivamente nas transformações I, II e III.
Nessas condições, é correto afirmar que
Na questão de Física, quando necessário, use:
• massa atômica do hidrogênio: mH = 1,67⋅10–27 kg
• massa atômica do hélio: mHe = 6,65⋅10–27 kg
• velocidade da luz no vácuo: c = 3⋅108 m/s
• constante de Planck: h = 6⋅10–34 J⋅s
• 1 eV = 1,6⋅10–19 J
• constante eletrostática do vácuo: k0 = 9,0⋅109 N⋅m2 / C2
• aceleração da gravidade: g = 10 m/s2
• cos 30º = sen 60º = √3/2
• cos 60º = sen 30º = 1/2
• cos 45º = sen 45º = √2/2
Considere uma dada massa gasosa de um gás perfeito que pode ser submetida a três transformações cíclicas diferentes I, II e III, como mostram os respectivos diagramas abaixo.
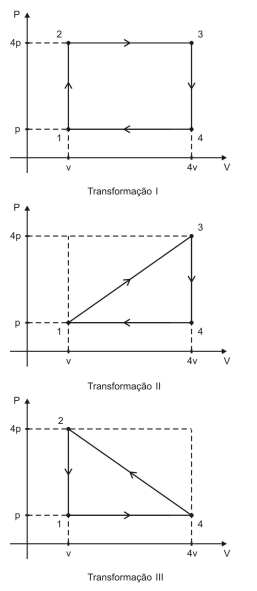
O gás realiza trabalhos totais 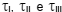 respectivamente
nas transformações I, II e III.
respectivamente
nas transformações I, II e III.
Nessas condições, é correto afirmar que
Uma amostra de um gás ideal sofre a transformação termodinâmica do estado A para o estado B representada no gráfico P (pressão) em função de T (temperatura) representada a seguir:
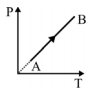
Entre as alternativas, assinale aquela que melhor representa o
gráfico P em função de V (volume) correspondente a
transformação termodinâmica de A para B.
Uma amostra de um gás ideal realiza uma sequência de transformações termodinâmicas (AB, BC, CD e DA) conforme o gráfico pressão (P) em função do volume (V) a seguir.
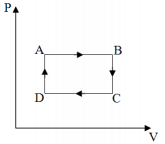
Assinale a alternativa que indica corretamente as
transformações termodinâmicas pelas quais a energia interna da
amostra aumentou.
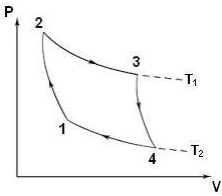
O Ciclo de Carnot, proposto no século XVIII pelo físico e engenheiro Nicolas Leonard Sadi Carnot, consiste em uma sequência de transformações gasosas, na qual uma máquina térmica, operando entre duas fontes térmicas, alcança rendimento máximo se operar em um ciclo totalmente reversível, independentemente da substância utilizada. Considerando o Ciclo de Carnot para um gás ideal, assinale a alternativa correta.
Considere uma máquina térmica que opera um ciclo termodinâmico que realiza trabalho.
A máquina recebe 400 J de uma fonte quente cuja temperatura é de 400 K e rejeita 200 J para uma fonte fria, que se encontra a 200 K. Neste ciclo a máquina térmica realiza um trabalho de 200 J.
• Analisando o ciclo termodinâmico exposto acima conclui-se que a máquina térmica é um ..I.. .
• Essa máquina térmica ..II.. a 1ª Lei da Termodinâmica.
• O rendimento desta máquina é ..III.. a 50%.
A opção que corresponde ao preenchimento correto das lacunas (I), (II) e (III) é:
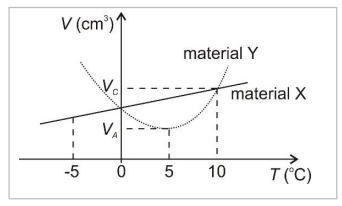
Com relação ao assunto, identifique como verdadeiras (V) ou falsas (F) as seguintes afirmativas:
( ) Os dois materiais têm mesma densidade em T = 0 ºC. ( ) À medida que a temperatura aumenta, o material Y se contrai até T = 10 ºC, e somente a partir dessa temperatura passa a dilatar-se. ( ) Em T = 5 ºC, um objeto maciço feito do material Y, se for colocado dentro de um recipiente contendo o material X, afunda quando sujeito apenas a forças gravitacionais e a forças exercidas pelo material X.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
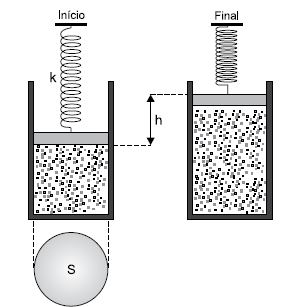
Desprezando todos os atritos e considerando 1 atm = 105 Pa, o deslocamento vertical h sofrido pelo pistão até atingir a posição final é de, aproximadamente,