Questões Militares
Comentadas sobre representação das transformações químicas em química
Foram encontradas 115 questões
A pólvora é material empregado como propulsor em armas de fogo. Basicamente, a ideia é provocar uma reação que gere uma quantidade grande de gases sob pressão e temperatura elevadas. Ao se expandirem, esses gases impulsionam um projétil. A pólvora negra, empregada em armas mais antigas, é constituída por uma mistura de salitre (KNO3), enxofre (S) e material de carbono (C). A equação não balanceada de uma das reações químicas que ocorrem durante a queima da pólvora é apresentada a seguir.
KNO3 (s) + S (s) + C (s) → K2S (s) + N2 (g) + CO2 (g)
Considerando essas informações e sabendo que o número atômico do carbono é igual a 6, julgue o item que se segue.
A menor soma de coeficientes estequiométricos inteiros que
permitem balancear a equação química apresentada é igual a 8.
A pólvora é material empregado como propulsor em armas de fogo. Basicamente, a ideia é provocar uma reação que gere uma quantidade grande de gases sob pressão e temperatura elevadas. Ao se expandirem, esses gases impulsionam um projétil. A pólvora negra, empregada em armas mais antigas, é constituída por uma mistura de salitre (KNO3), enxofre (S) e material de carbono (C). A equação não balanceada de uma das reações químicas que ocorrem durante a queima da pólvora é apresentada a seguir.
KNO3 (s) + S (s) + C (s) → K2S (s) + N2 (g) + CO2 (g)
Considerando essas informações e sabendo que o número atômico do carbono é igual a 6, julgue o item que se segue.
Entre os produtos da reação química apresentada, podem ser
identificadas uma substância iônica e duas substâncias
moleculares; entre as substâncias moleculares, uma é polar e,
a outra, apolar.
Com relação a reações químicas e a substâncias, julgue o item subsequente.
No balanceamento de uma equação química, o número
de substâncias no reagente tem que ser igual ao número
de substâncias no produto.
Acerca dos diferentes tipos de ligações químicas e das substâncias formadas em reações químicas, julgue o próximo item.
Nas moléculas, os átomos das substâncias são organizados
linearmente de acordo com sua fórmula molecular.
A respeito da matéria e de sua constituição química, julgue o item a seguir.
A massa molecular das substâncias é dada pela soma das
massas de todos os átomos que constituem suas moléculas
ou fórmulas mínimas.
A respeito da matéria e de sua constituição química, julgue o item a seguir.
O mol é a unidade de medida da grandeza quantidade
de matéria.
Na ânsia pelo "elixir da longa vida", por volta do século I, alquimistas descobriram acidentalmente a Pólvora, referenciada em textos de Alquimia pelos avisos quanto aos cuidados para não se misturarem certos materiais uns com os outros. A pólvora, mais conhecida desde o final do século XIX como pólvora negra, é uma mistura química que queima com rapidez. Foi extensamente utilizada como propelente em canhões e armas de fogo e atualmente ainda é empregada em artefatos pirotécnicos. Nitrato de potássio, enxofre e carvão (carbono) são os constituintes da pólvora negra. Sobre as espécies constituintes da pólvora negra afirma-se que
Dados:
Número Atômico: K = 19; N = 7; O = 8; S = 16; C = 6
I - o nitrato de potássio é classificado como uma base segundo a teoria de Arrhenius;
II - a 25 °C e 1 atm a variedade alotrópica mais estável do carbono é a grafite e a do enxofre é a rômbica;
III - a fórmula do nitrato de potássio é KNO2 ;
IV - o enxofre é um metal radioativo que pertence à família 6A (16) da tabela periódica;
V - o átomo de carbono (6C) estabelece 4 ligações químicas e possui a variedade alotrópica diamante, substância natural de alta dureza;
Estão corretas apenas as afirmativas
A emissão de gases derivados do enxofre, como o dióxido de enxofre (SO2), pode ocasionar uma série de problemas ambientais e a destruição de materiais como rochas e monumentos à base de calcita (carbonato de cálcio). Essa destruição ocasiona reações com a emissão de outros gases, como o gás carbônico (CO2), potencializando o efeito poluente. Considerando as equações das reações sucessivas a 27 °C e 1 atm, admitindo-se os gases como ideais e as reações completas, o volume de CO2 produzido a partir da utilização de 2 toneladas de SO2 como reagente é, aproximadamente,
Dados
Massas Atômicas: S = 32 u ; O = 16 u ; H = 1 u ; C = 12 u ; Ca = 40 u
Constante dos gases ideais: R = 0,082 atm L
L mol-1
mol-1 K-1
K-1
Volume molar nas condições em que ocorreu a reação (27° e 1 atm) = 24,6 L/mol
SO2 (g) + 1/2 O2 (g) → SO3 (g) (equação I)
SO3 (g) + H2O (ℓ) → H2SO4 (ℓ) (equação II)
H2SO4 (ℓ) + CaCO3 (s) → CaSO4 (s) + H2O (ℓ) + CO2 (g) (equação III)
Em ambientes fechados, o superóxido de potássio (KO2) é utilizado em máscaras de respiração, para remover o dióxido de carbono e a água do ar exalado. A remoção de água gera oxigênio para a respiração por meio da reação
4KO2(s) + 2H2O(l) → 3O2(g) + 4KOH(s). (I)
O hidróxido de potássio remove o dióxido de carbono da máscara pela reação
KOH(s) + CO2(g) → KHCO3(s). (II)
P. W. Atkins e L. Jones. Princípios de química. Rio de Janeiro: LTC, 2006, p. 125.
Com base nas informações acima, julgue o próximo item.
Considerando a proporção estequiométrica entre as
substâncias envolvidas na reação representada pela
equação I, conclui-se que cada mol de superóxido de
potássio, ao reagir com quantidade suficiente de água,
produz 0,75 mol de gás oxigênio.
Bebidas especialmente ingeridas por esportistas têm representado importante fatia de consumo. Tais bebidas são soluções isotônicas repositoras hidroeletrolíticas e, portanto, auxiliam na manutenção e preparação física de atletas de todas as modalidades. A seguir, reproduz-se parte da tabela nutricional constante no rótulo de uma dessas bebidas.

A partir dessas informações e considerando os múltiplos aspectos que
elas suscitam, julgue o item subsequente.
Considerando-se o valor aproximado de 6×1023 mol-1 para a
constante de Avogadro, conclui-se que é superior a 3×1020 a
quantidade de íons potássio presente em 1 copo de 200 mL da
referida bebida isotônica.
Leia as informações da tabela a seguir que representa alguns ácidos e suas aplicações.
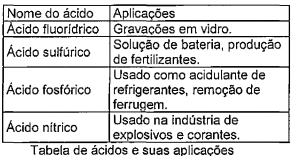
As fórmulas dos ácidos citados na tabela acima são,
respectivamente:
CrCl3 + NaOH + H2O2 → Na2CrO4 + NaCl + H2O
Butano é o gás armazenado em botijões ou encanamentos, usado no cozimento dos alimentos.
O gás butano, derivado do petróleo, é uma substância inodora e incolor. Devido a essas características outros elementos costumam ser acrescentados ao butano, para que, em caso de vazamento, possa se sentir o cheiro e evitar possíveis acidentes.

A combustão completa desse gás produz gás carbônico e água segundo a equação não balanceada a seguir
C4H10(g) + O2(g) → CO2(g) + H2O(l)
O balanceamento correto dessa equação permite concluir que,
para cada molécula de butano queimada, há produção de
Uma das aplicações da trinitroglicerina, cuja fórmula é C3H3N3O9, é a confecção de explosivos. Sua decomposição enérgica gera como produtos os gases nitrogênio, dióxido de carbono e oxigênio, além de água, conforme mostra a equação da reação a seguir:
4 C3H3N3O9 (l) → 6 N2 (g) + 12 CO2 (g) + 1 O2 (g) + 10 H2O (l).
Além de explosivo, a trinitroglicerina também é utilizada como princípio ativo de medicamentos no tratamento de angina, uma doença que acomete o coração. Medicamentos usados no tratamento da angina usam uma dose padrão de 0,6 mg de trinitroglicerina na formulação. Considerando os dados termoquímicos da reação a 25 ºC e 1 atm e supondo que essa massa de trinitroglicerina sofra uma reação de decomposição completa, a energia liberada seria aproximadamente de
Dados: massas atômicas: C = 12 u; H = 1 u; N = 14 u; O = 16 u.
∆Hof (H2O) = - 286 kJ/mol; ∆Hof
(CO2) = - 394 kJ/mol; ∆Hof
(C3H5N3O9) = - 353,6 kJ/mol
Um mineral muito famoso, pertencente ao grupo dos carbonatos, e que dá origem a uma pedra semipreciosa é a malaquita, cuja a fórmula é: Cu2(OH)2CO3 (ou CuCO3.Cu(OH)2).
Experimentalmente pode-se obter malaquita pela reação de precipitação que ocorre entre soluções aquosas de sulfato de cobre II e carbonato de sódio, formando um carbonato básico de cobre II hidratado, conforme a equação da reação:
2 CuSO4 (aq) + 2 Na2CO3 (aq) + H2O (l) → CuCO3.Cu(OH)2 (s) + 2 Na2SO4 (aq) + CO2 (g)
Na reação de síntese da malaquita, partindo-se de 1060 g de carbonato de sódio e considerando-se um rendimento de reação de 90%, o volume de CO2 (a 25 ºC e 1 atm) e a massa de malaquita obtida serão, respectivamente, de:
Dados: – massas atômicas Cu = 64 u; S = 32 u; O = 16 u; Na = 23 u; C = 12 u; H = 1 u.
– volume molar 24,5 L/mol, no estado padrão.