Questões Militares
Comentadas sobre substâncias e suas propriedades em química
Foram encontradas 246 questões
A pólvora é material empregado como propulsor em armas de fogo. Basicamente, a ideia é provocar uma reação que gere uma quantidade grande de gases sob pressão e temperatura elevadas. Ao se expandirem, esses gases impulsionam um projétil. A pólvora negra, empregada em armas mais antigas, é constituída por uma mistura de salitre (KNO3), enxofre (S) e material de carbono (C). A equação não balanceada de uma das reações químicas que ocorrem durante a queima da pólvora é apresentada a seguir.
KNO3 (s) + S (s) + C (s) → K2S (s) + N2 (g) + CO2 (g)
Considerando essas informações e sabendo que o número atômico do carbono é igual a 6, julgue o item que se segue.
Entre os produtos da reação química apresentada, podem ser
identificadas uma substância iônica e duas substâncias
moleculares; entre as substâncias moleculares, uma é polar e,
a outra, apolar.
Com relação a reações químicas e a substâncias, julgue o item subsequente.
Um átomo de carbono pode formar 2, 4 ou 6 ligações com
outro átomo de carbono.
Acerca dos diferentes tipos de ligações químicas e das substâncias formadas em reações químicas, julgue o próximo item.
Em uma ligação covalente, os elétrons são cedidos pelo átomo
de maior tamanho.
Acerca dos diferentes tipos de ligações químicas e das substâncias formadas em reações químicas, julgue o próximo item.
As ligações iônicas são formadas pela união de íons com
cargas iguais.
Com relação ao funcionamento desses tipos de extintores e aos seus componentes químicos, julgue o item a seguir.
A substância do extintor de pó químico é formada por ligações
covalentes e iônicas.
"Sempre que uma substância muda de fase de agregação, a temperatura permanece constante enquanto a mudança se processa, desde que a pressão permaneça constante".
FONSECA Martha Reis Marques da, Química Geral, São Paulo: Ed FTD, 2007, pág 41.
O gráfico abaixo representa a mudança de fase de agregação de uma substância pura com o passar do tempo, em função da variação de temperatura, observada ao se aquecer uma substância X durante algum tempo, sob pressão constante.
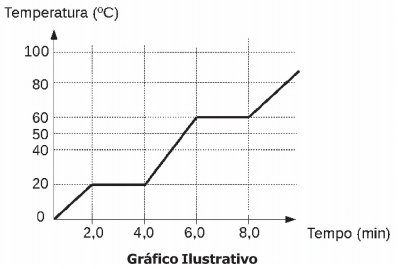
Tomando-se como base o gráfico, analise as seguintes afirmativas:
I - entre 0 °C e 19 °C, a substância X encontra-se na fase sólida;
II - o intervalo de 2,0 min a 4,0 min corresponde à condensação da substância X;
III - a temperatura de 60 °C corresponde à temperatura de ebulição da substância X;
IV - no intervalo de 40 °C a 50 °C, a substância X encontra-se na fase líquida.
Estão corretas apenas as afirmativas
Conversores catalíticos (catalisadores) de automóveis são utilizados para reduzir a emissão de poluentes tóxicos. Poluentes de elevada toxicidade são convertidos a compostos menos tóxicos. Nesses conversores, os gases resultantes da combustão no motor e o ar passam por substâncias catalisadoras. Essas substâncias aceleram, por exemplo, a conversão de monóxido de carbono (CO) em dióxido de carbono (CO2) e a decomposição de óxidos de nitrogênio como o NO, N2O e o NO2 (denominados NOx) em gás nitrogênio (N2) e gás oxigênio (O2). Referente às substâncias citadas no texto e às características de catalisadores, são feitas as seguintes afirmativas:
I - a decomposição catalítica de óxidos de nitrogênio produzindo o gás oxigênio e o gás nitrogênio é classificada como uma reação de oxidorredução;
II - o CO2 é um óxido ácido que, ao reagir com água, forma o ácido carbônico;
III - catalisadores são substâncias que iniciam as reações químicas que seriam impossíveis sem eles, aumentando a velocidade e também a energia de ativação da reação;
IV - o CO é um óxido básico que, ao reagir com água, forma uma base;
V - a molécula do gás carbônico (CO2) apresenta geometria espacial angular.
Das afirmativas feitas estão corretas apenas a
Considere os seguintes processos:
I- Atração do ferro pelo ímã.
II- Combustão da gasolina.
III- Desaparecimento de bolinhas de naftalina.
IV- Enferrujamento de um prego.
São processos químicos somente
Ao aquecer o iodo num béquer coberto com o vidro de relógio, após certo tempo observa-se que seus vapores ficaram roxos.
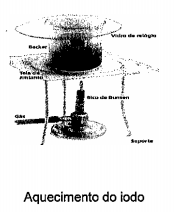
Esse fenômeno é uma mudança de estado físico chamada
Observe a figura a seguir que apresenta a aparelhagem utilizada comumente em laboratórios para a realização da destilação simples.
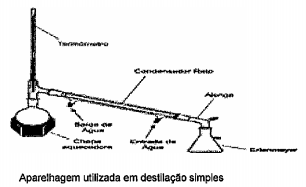
Marque a opção que apresenta a mistura que pode ser
separada por essa aparelhagem.
“A matéria pode ser definida de maneira bem simplificada como sendo tudo aquilo que tem massa e volume e ocupa um lugar no espaço. Portanto, a matéria é constituída de minúsculas partículas, que podem ser átomos, moléculas, íons e assim por diante. De modo que, simplificadamente, o que diferencia um estado físico de outro é a organização dessas partículas, se elas estão mais próximas umas às outras ou mais afastadas, isto é, se estão mais agregadas ou menos agregadas. Por isso, os estados físicos podem ser corretamente chamados de ‘estados de agregação’.”
(Disponível em: http://manualdaquimica.uol.com.br/quimica-geral/estados-fisicos-materia.htm. Acesso em: 08 de junho de 2017.)
Sobre os estados de agregação, analise as afirmativas a seguir.
I. Nesse estado, as partículas estão bem próximas umas às outras, de modo que não se movimentam. Estão bem organizadas e, por isso, possuem forma e volume fixos, não podendo sofrer compressão.
II. Nesse estado, as partículas possuem menor liberdade de movimentação que no estado sólido, pois estão um pouco mais afastadas umas das outras, havendo certo espaço entre elas. Por essa razão, as substâncias líquidas, como a água, possuem forma variável, adaptando-se ao recipiente em que estão contidas, mas não podem ser comprimidas, pois possuem volume constante.
III. Nesse estado, as partículas estão bem afastadas umas das outras, possuindo grande liberdade de movimentação. Por isso, os gases e os vapores, como o vapor de água, não possuem forma nem volume fixos, conformando-se de acordo com o recipiente e podendo ser comprimidos.
Sobre os estados físicos estão corretas as afirmativas
Acerca da petroquímica, área da química responsável pelas reações químicas envolvendo o petróleo, o petróleo deve passar por processos para que o seu aproveitamento energético seja possível: separação, conversão e tratamento. Sobre esses processos, analise as afirmativas a seguir.
I. O processo de separação é aquele que isola as famílias de hidrocarbonetos realizando o que se chamam frações, sem qualquer reação química.
II. No processo de conversão ocorrem diversas reações químicas nas frações e são gerados novos grupos de hidrocarbonetos.
III. No processo de tratamento são eliminadas quaisquer impurezas nas frações e no óleo cru, através de conversões químicas.
Estão corretas as afirmativas
Observe a figura a seguir.
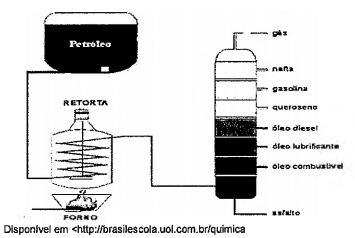
O petróleo bruto é uma complexa mistura líquida de compostos orgânicos, denominados hidrocarbonetos, que vão desde os alcanos mais simples até aos aromáticos mais complexos, dando origem à gasolina, ao querosene, ao óleo combustível, ao óleo diesel, ao óleo lubrificante e também a substâncias que serão posteriormente transformadas pela indústria petroquímica em plásticos, fertilizantes, vernizes e fios para tecelagem, conforme a figura acima.
O processo que permite a separação dessas substâncias
a partir do petróleo bruto é conhecido como
Considere os sistemas abaixo.
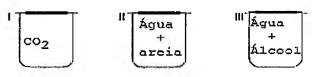
Os sistemas I, II e III correspondem, respectivamente, à
substância
Analise os compostos a seguir de acordo com suas propriedades de ligação entre moléculas.
I. Metano.
II. Monóxido de carbono.
III. Ácido clorídrico.
IV. Gás cloro.
As alternativas que contêm somente moléculas apolares são: