Questões Militares
Comentadas sobre substâncias inorgânicas e suas características: ácidos, bases, sais e óxidos. reações de neutralização. em química
Foram encontradas 63 questões
Conversores catalíticos (catalisadores) de automóveis são utilizados para reduzir a emissão de poluentes tóxicos. Poluentes de elevada toxicidade são convertidos a compostos menos tóxicos. Nesses conversores, os gases resultantes da combustão no motor e o ar passam por substâncias catalisadoras. Essas substâncias aceleram, por exemplo, a conversão de monóxido de carbono (CO) em dióxido de carbono (CO2) e a decomposição de óxidos de nitrogênio como o NO, N2O e o NO2 (denominados NOx) em gás nitrogênio (N2) e gás oxigênio (O2). Referente às substâncias citadas no texto e às características de catalisadores, são feitas as seguintes afirmativas:
I - a decomposição catalítica de óxidos de nitrogênio produzindo o gás oxigênio e o gás nitrogênio é classificada como uma reação de oxidorredução;
II - o CO2 é um óxido ácido que, ao reagir com água, forma o ácido carbônico;
III - catalisadores são substâncias que iniciam as reações químicas que seriam impossíveis sem eles, aumentando a velocidade e também a energia de ativação da reação;
IV - o CO é um óxido básico que, ao reagir com água, forma uma base;
V - a molécula do gás carbônico (CO2) apresenta geometria espacial angular.
Das afirmativas feitas estão corretas apenas a
Em ambientes fechados, o superóxido de potássio (KO2) é utilizado em máscaras de respiração, para remover o dióxido de carbono e a água do ar exalado. A remoção de água gera oxigênio para a respiração por meio da reação
4KO2(s) + 2H2O(l) → 3O2(g) + 4KOH(s). (I)
O hidróxido de potássio remove o dióxido de carbono da máscara pela reação
KOH(s) + CO2(g) → KHCO3(s). (II)
P. W. Atkins e L. Jones. Princípios de química. Rio de Janeiro: LTC, 2006, p. 125.
Com base nas informações acima, julgue o próximo item.
A equação II representa a reação entre uma base forte e um
óxido ácido, da qual resulta o sal carbonato de potássio
Em ambientes fechados, o superóxido de potássio (KO2) é utilizado em máscaras de respiração, para remover o dióxido de carbono e a água do ar exalado. A remoção de água gera oxigênio para a respiração por meio da reação
4KO2(s) + 2H2O(l) → 3O2(g) + 4KOH(s). (I)
O hidróxido de potássio remove o dióxido de carbono da máscara pela reação
KOH(s) + CO2(g) → KHCO3(s). (II)
P. W. Atkins e L. Jones. Princípios de química. Rio de Janeiro: LTC, 2006, p. 125.
Com base nas informações acima, julgue o próximo item.
A análise da estrutura do superóxido de potássio demonstra
que ele é uma substância de natureza molecular.
Bebidas especialmente ingeridas por esportistas têm representado importante fatia de consumo. Tais bebidas são soluções isotônicas repositoras hidroeletrolíticas e, portanto, auxiliam na manutenção e preparação física de atletas de todas as modalidades. A seguir, reproduz-se parte da tabela nutricional constante no rótulo de uma dessas bebidas.

A partir dessas informações e considerando os múltiplos aspectos que
elas suscitam, julgue o item subsequente.
Os cloretos de sódio e de potássio podem ser preparados por
meio da neutralização total do ácido clórico com hidróxidos de
sódio e de potássio, respectivamente.
CrCl3 + NaOH + H2O2 → Na2CrO4 + NaCl + H2O
Conversores catalíticos de automóveis são utilizados para reduzir a emissão de poluentes. Os gases resultantes da combustão no motor e o ar passam por substâncias catalisadoras que aceleram a transformação de monóxido de carbono (CO) em dióxido de carbono (CO2) e a decomposição de óxidos de nitrogênio (genericamente NxOy) em gás nitrogênio (N2) e gás oxigênio (O2). Em relação ao uso de catalisadores e as substâncias citadas no texto, são feitas as seguintes afirmações:
I – As reações de decomposição dos óxidos de nitrogênio a gás oxigênio e a gás nitrogênio ocorrem com variação no número de oxidação das espécies.
II – O CO2 é um óxido ácido que quando reage com a água forma o ácido carbônico.
III – Catalisadores são substâncias que iniciam as reações químicas que seriam impossíveis sem eles, aumentando a velocidade e também a energia de ativação da reação.
IV – O monóxido de carbono é um óxido básico que ao reagir com a água forma uma base.
V – A molécula do gás carbônico apresenta geometria espacial angular.
Das afirmativas feitas estão corretas apenas:
A chuva ácida é um fenômeno químico resultante do contato entre o vapor de água existente no ar, o dióxido de enxofre e os óxidos de nitrogênio. O enxofre é liberado, principalmente, por veículos movidos a combustível fóssil; os óxidos de nitrogênio, por fertilizantes. Ambos reagem com o vapor de água, originando, respectivamente, os ácidos sulfuroso, sulfídrico, sulfúrico e nítrico.
Assinale a opção que apresenta, respectivamente, a fórmula desses ácidos.
Em 2012, uma carreta carregada com ácido sulfúrico (H2 SO4 ) tombou na Br-381. Sabe-se que o ácido sulfúrico tem as seguintes propriedades:

Considerando que nesse acidente o derramamento de ácido foi de 20 mil litros, qual a massa, em gramas,
aproximada de bicarbonato de sódio (NaHCO3
) necessária para neutralizar totalmente o ácido?
O rótulo de uma garrafa de água mineral apresenta a seguinte descrição:
COMPOSIÇÃO QUÍMICA PROVÁVEL (mg/L): bicarbonato de bário = 0,38; bicarbonato de estrôncio = 0,03; bicarbonato de cálcio = 66,33; bicarbonato de magnésio = 50,18; bicarbonato de potássio = 2,05; bicarbonato de sódio = 3,04; nitrato de sódio = 0,82; cloreto de sódio = 0,35.
CARACTERÍSTICAS FÍSICO-QUÍMICAS: pH medido a 25 °C = 7,8; temperatura da água na fonte = 18 °C; condutividade elétrica a 25 °C = 1,45·10-4 mhos/cm; resíduo de evaporação a 180 °C = 85,00 mg/L; radioatividade na fonte a 20 °C e 760 mm Hg = 15,64 maches.
A respeito da água mineral citada, de sua composição e características, são feitas as seguintes afirmativas:
I – esta água apresenta caráter básico nas condições citadas.
II – a água mineral citada pode ser classificada como uma solução, em razão da presença de substâncias dissolvidas.
III – todas as substâncias químicas presentes na composição provável apresentada são da função inorgânica Sal.
1. Caráter básico.
2. Caráter anfótero.
3. Caráter neutro.
4. Caráter ácido.
( ) CO, NO, N2O.
( ) Como regra, óxidos de elementos localizados à esquerda na tabela periódica.
( ) ZnO e Al2O3.
( ) Como regra, óxidos de elementos com alta eletronegatividade.
A sequência está correta em
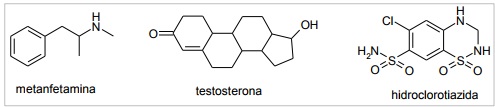
Sobre as substâncias utilizadas em doping, apresentadas na questão anterior, considere as seguintes afirmativas:
1. A metanfetamina possui uma amina secundária.
2. A testosterona é um composto aromático.
3. A testosterona possui função cetona.
4. A hidroclorotiazida é um sal.
Assinale a alternativa correta.
Qual das opções apresenta a equação de uma reação que NÃO acontece pela ação estomacal desse medicamento?
( ) Ao adicionar solução de fenolftaleína em um meio ácido a solução ficará incolor, pois o aumento da concentração de H+ desloca o equilíbrio.
( ) O ácido carbônico é um ácido fraco, extremamente instável, que se forma somente em equilíbrio dinâmico entre a água e o gás carbônico.
( ) Quando reagem com o zinco produzem hidrogênio gasoso.
( ) Reagem com carbonatos e bicarbonatos para produzir monóxido de carbono.
A sequência está correta em
Em relação à concentração de uma das espécies resultante na mistura final, é CORRETO afirmar que
O bicarbonato de sódio pode ser classificado como sal