Questões Militares
Comentadas sobre transformações químicas e energia em química
Foram encontradas 267 questões
Analise as afirmativas acerca das equações termoquímicas descritas por Masterton (2010).
I. O valor em módulo ΔH é diretamente proporcional às quantidades dos reagentes ou dos produtos.
II. O valor de ΔH para uma reação é igual ao de seu valor em reação inversa.
III. O valor de ΔH para uma reação é o mesmo independente se ela ocorra em uma ou em uma série de etapas.
Estão corretas as afirmativas
Acerca da radioatividade, analise as afirmativas a seguir:
I. Possui o dobro da carga de um próton, ou seja, +2.
II. São elétrons emitidos dos núcleos dos átomos.
III. Tem grade poder de penetração, superior até 15 cm no aço.
IV. Tem velocidade igual à da luz.
Corresponde apenas às partículas betas a afirmativa
A afirmativa a seguir contextualiza a questão. Leia‐a atentamente.
“A corrosão é a deterioração de um material, geralmente metálico, por ação química ou eletroquímica do meio ambiente associada ou não a esforços mecânicos.”
(GENTIL, V. corrosão. LTC. 6ª ed. 2012.)
Nem sempre é possível, nem de interesse, ter as concentrações iônicas a 1M ou atividade unitária, por isso se utiliza certa equação para poder fazer o cálculo da determinação dos novos potenciais. Esta equação foi desenvolvida por qual cientista?“A meia-vida de um elemento radioativo é o intervalo de tempo em que uma amostra deste elemento se reduz à metade. Este intervalo de tempo também é chamado de período de semidesintegração. À medida que os elementos radioativos vão se desintegrando, no decorrer do tempo, a sua quantidade e atividade vão reduzindo e, por consequência, a quantidade de energia emitida por ele, em razão da radioatividade, também é reduzida.”
(ALMEIDA, Frederico Borges de. “Meia-Vida”; Brasil Escola. Disponível em http://brasilescola.uol.com.br/fisica/meiavida.htm. Acesso em: 24 de fevereiro de 2017.)
Assinale a alternativa que corresponde à massa residual de um material radioativo, que continha 10 g iniciais, após ter sua terceira meia-vida.
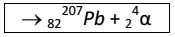
2 H₂O + O₂ + 4 e⁻ ↔ 4OH⁻ E° = +0,401 V
Sendo P₀₂ catodo e P₀₂ anodo as pressões parciais do oxigênio no catodo e no anodo respectivamente, é correto afirmar que o potencial da pilha é:
Muitos radioisótopos decaem basicamente de maneira completa em questão de segundos ou menos, de forma que não os encontramos na natureza. O urânio-238, por outro lado, decai muito lentamente; por isso, apesar de sua instabilidade, ainda podemos observá-lo na natureza. Uma importante característica de um radioisótopo é sua velocidade de decaimento. Sobre cinética da desintegração nuclear, analise as afirmativas a seguir.
(Considere: ln 4,5x10–5 = –10,00
ln 0,77 = –0,26
e –11,53 = 9,8 x10–6 .)
I. Uma rocha contém 0,257 mg de chumbo-206 para cada miligrama de urânio-238. A meia vida para o decaimento de urânio-238 a chumbo-206 é 4,5 x 109 anos. A idade da rocha é 1,7 x 109 ano.
II. A constante de velocidade da desintegração α do 86Rn222 é 0,18 dia–1 . A quantidade que será reduzida a massa de 4,5 x 10–5 g desse nuclídeo, depois de um período de 8,5 dias é 9,8 x 10–6 g.
III. À medida que uma amostra radioativa decai, a quantidade de radiação que emana da amostra também decai. A meia-vida do cobalto-60 é 5,26 anos. A amostra de 4,0 mCi de cobalto-60 teria, após 5,26 anos, uma atividade de radiação de 3,7 x 1010 Bq.
Está(ão) correta(s) apenas a(s) afirmativa(s)
Reações de oxidação e redução podem ocorrer em muitos sistemas químicos. Exemplos incluem nosso próprio sistema respiratório e o sistema fotossintético complementar nas plantas. Além disso, podemos pensar no processo de assar o pão, no enferrujamento do ferro, na ação dos alvejantes sobre as manchas e na produção e combustão do petróleo. Nesse contexto, analise as afirmativas a seguir.
I. O ∆G° para a reação NiO2(s) + 2Cl– (aq) + 4H+ (aq) → Cl2(g) + Ni2+(aq) + 2H2O, sabendo que o potencial padrão de pilha é 0,320 V a 25°C é –30,9 kJ.
II. 0,395 g de cobre são depositados no catodo de uma célula eletrolítica se uma corrente elétrica de 2,00 A passa por uma solução de CuSO4 por um período de 20 min.
III. Na eletrólise de solução aquosa de cloreto de sódio forma-se gás cloro no ânodo e gás hidrogênio no cátodo.
Está(ão) correta(s) apenas a(s) afirmativa(s)