Questões de Concurso Militar CIAAR 2017 para Primeiro Tenente - Engenharia Química
Foram encontradas 60 questões
Os confinamentos nos quais ocorrem reações químicas são chamados reatores. Existem vários tipos de reatores químicos e várias maneiras de classificá-los.
Informe se é verdadeiro (V) ou falso (F) o que se afirma abaixo sobre Reatores.
( ) O reator em batelada é um tipo de vaso largamente usado em processos industriais. As vantagens de um reator de batelada residem em sua versatilidade.
( ) Reator perfeitamente agitado (RPA) é um tipo de reator ideal comum em engenharia química. Frequentemente refere-se a um modelo usado para estimar as variáveis principais de uma operação unitária.
( ) Reator de fluxo em pistão (PFR) é usado para descrever reações químicas em sistemas de fluxo contínuo.
( ) A manutenção de reatores RPA é mais cara do que a manutenção dos reatores RFP.
( ) Reatores de fluxo em pistão têm uma conversão por unidade de volume baixa, mas operam por longos períodos de tempo sem manutenção.
A alternativa que apresenta a sequência correta é
Um catalisador é uma substância que faz variar a velocidade de uma reação química sem que ele próprio sofra uma variação química permanente no processo. Os catalisadores são bem comuns, muitas reações na indústria química ocorrem com a ajuda de catalisadores.
Informe se é verdadeiro (V) ou falso (F) o que se afirma abaixo sobre a Catálise Homogênea.
( ) Os catalisadores podem agir aumentando a velocidade de reação, mas não alteram o número de colisões efetivas.
( ) Os átomos de cloro são catalisadores para a destruição do ozônio.
( ) Na ausência do catalisador, as reações ocorrem de maneira extremamente lenta.
A alternativa que apresenta a sequência correta é
O gráfico a seguir representa a variação de concentração das espécies A, B e C com o tempo:
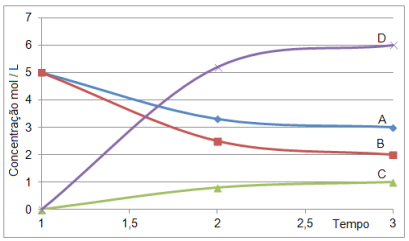
Mediante a reação representada pelo gráfico, marque a alternativa que representa corretamente a equação
química.
Uma amostra de gás ideal sofreu uma transformação termodinâmica à pressão constante igual a 30 N/m2 . O volume e a temperatura absoluta variam como indica o gráfico a seguir.
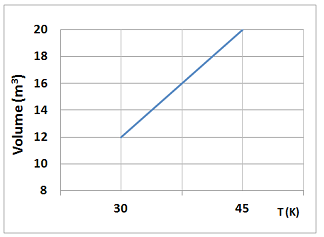
Sabendo-se que, nessa transformação, o gás absorve 400J de calor, pode-se afirmar que a variação de sua
energia interna é de
Informe se é verdadeiro (V) ou falso (F) o que se afirma abaixo sobre as propriedades termodinâmicas.
( ) Ponto de orvalho é a temperatura na qual se inicia a condensação da mistura.
( ) Ponto de bolha é a temperatura na qual se inicia a ebulição do líquido puro.
( ) Quando a mistura está no ponto de bolha, dizemos que é um líquido insaturado.
( ) Se a mistura estiver aquecida acima do ponto de bolha, dizemos que é vapor superaquecido
A alternativa que apresenta a sequência correta é
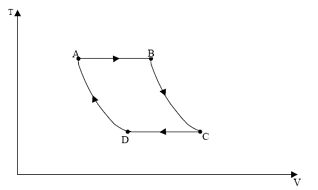
Com base nesse gráfico, é correto afirmar que entre os pontos
A nitroglicerina é um líquido oleoso de cor amarelo-pálida. É altamente sensível ao choque. O simples ato de balançar o líquido pode causar a explosiva decomposição em gases de nitrogênio, dióxido de carbono, água e oxigênio. A equação química abaixo representa essa reação.
4C3H5N3O9 (l ) → 6N2 (g ) + 12CO2 (g ) + 10H2O (g ) + O2 (g )
Calcule o volume de gases CO2 produzido quando uma amostra de 200 gramas de nitroglicerina é detonada. Considere os seguintes dados: Massa g/mol: H = 1; C = 12; N = 14; O = 16; Constante universal dos gases: R = 8,2 · 10−2 atm · L · K−1 · mol−1; Pressão: 1 atm; Temperatura: 27°C e Volume Molar: 22,4 L . mol-1.
Mediante análise, marque a alternativa que apresenta corretamente o volume aproximado.
Para misturas binárias, as condições de equilíbrio para várias composições podem ser facilmente visualizadas em diagramas do tipo Txy e xy, à pressão constante, ou Pxy e xy, à temperatura constante.
Diagrama binário para a mistura Benzeno e Tolueno.
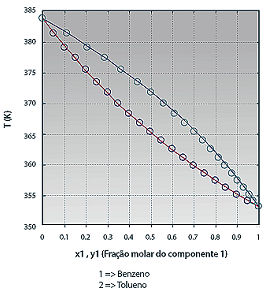
(Disponível em: <http://labvirtual.eq.uc.pt> )
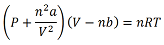
Na equação, as variáveis P, V, n, R, T são usuais, mas os parâmetros (a) e (b) são conhecidos como constantes de Van Der Waals.
Considerar R: 0,0821 atm · L · K−1 · mol−1
Tabela – Constantes de Van Der Waals
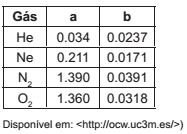
Utilizando a equação de Van Der Waals para gases reais, calcule a pressão real exercida por 16 gramas de gás oxigênio que se encontra em um recipiente de 1L a 27°C.
Muitos foram os pesquisadores que contribuíram para as leis conhecidas como Leis dos Gases. Algumas das contribuições mais importantes dos gases ideais estão resumidas nos postulados na lei de Boyle, lei de Charles, lei de Gay-Lussac e lei de Clapeyron. Com relação às leis dos gases, analise as afirmativas a seguir.
I. De acordo com a lei de Boyle, a pressão e o volume de um gás são inversamente proporcionais entre si para um gás ideal.
II. De acordo com a lei de Gay-Lussac, a velocidade de difusão e de efusão de um gás é inversamente proporcional à raiz quadrada de sua densidade.
III. De acordo com a lei de Charles, o volume de um gás é diretamente proporcional à sua temperatura absoluta.
IV. De acordo com a lei de Clapeyron, à volume constante, a pressão de uma certa massa constante de um gás é proporcional à temperatura absoluta a qual está submetida.
Está correto apenas o que se afirma em
A cavitação é um fenômeno indesejado no funcionamento das máquinas de fluxo e ocorre em regiões de altas velocidades e baixa pressão dos tubos de sucção em máquinas motoras e geradoras. Ela pode provocar corrosão, desgaste, remoção de partículas e destruição de partes dos rotores das bombas. Tal circunstância faz com que as condições de sucção tenham papel importante no projeto e nas especificações das instalações para o correto funcionamento, tanto de bombas quanto de turbinas.
Com relação ao funcionamento de máquinas de fluxo e o fenômeno da cavitação, marque a alternativa correta.
Inibidor de corrosão é uma substância ou mistura de substâncias que, quando presente em concentrações adequadas, no meio corrosivo, reduz ou elimina a corrosão. As seguintes afirmativas referem-se ao inibidor de corrosão.
I. Inibidores protetivos emulsionáveis em água deixam por evaporação uma película oleosa aplicada por diluição em água.
II. O método de proteção usando protetivos temporários é baseado na obtenção de uma película superficial, fácil de aplicar e remover.
III. Inibidores catódicos têm a capacidade de formar películas sobre as áreas anódicas e catódicas, interferindo com a ação eletroquímica.
IV. Inibidores anódicos atuam favorecendo as reações anódicas, protegendo o cátodo da corrosão. São eficazes, mesmos em pequenas concentrações.
Está correto apenas o que se afirma em
Corrosão é a destruição ou deterioração de um material devido à reação química ou eletroquímica com seu meio. A corrosão é a transformação de um material pela sua interação química ou eletroquímica com o meio.
Sobre os exemplos de métodos de combate à corrosão, é incorreto afirmar que
A Equação de Nernst, desenvolvida pelo químico e físico alemão Walther Hermann Nernst, é a relação quantitativa que permite calcular a força eletromotriz de uma pilha para concentrações de íons diferentes de uma unidade. Também é usada para cálculos em titulação de oxidação-redução.
A equação a 25°C pode ser escrita de forma reduzida como: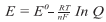
Sendo: R = 8,315 J K-1 mol-1; T = 298,2 K (25°C); F = 96485 C mol-1
Calcule a força eletromotriz para a seguinte pilha a 25°C: Fe / Fe2 + (0,02M) || Cu2
+(0,2M) / Cu
Dados: potencial padrão de redução (Eº Fe = -0,44V e Eº Cu = +0,40V).