Questões de Concurso Militar CIAAR 2018 para Primeiro Tenente - Engenharia Química
Foram encontradas 9 questões
O saturador adiabático é um equipamento utilizado para umidificar o ar em um processo industrial. Esse equipamento consiste de uma câmara contendo água no estado líquido sobre a qual passa uma corrente de ar. A água evapora adiabaticamente e, assim, o ar que entra seco no equipamento, sai umidificado. Considerando um saturador adiabático que possua uma câmara que comporta 5.000cm3 de água e com uma altura h de 500cm. Ar seco entra no equipamento e, após umidifcado, sai com água a uma concentração igual a 50% da saturação, a uma velocidade constante, sem que haja perturbações na superfície da água. O nível da água é mantida constante devido ao bombeamento de 20cm3 .h-1 de água para dentro da câmara. O sistema opera a 25°C (298K) e 101kPa. O coeficiente de difusão da água no ar é igual a 900cm2 .h-1, a densidade da água líquida é 1,0g.cm-3, a massa molar da água é 18g.mol-1 e a pressão de vapor da água 3,17kPa.
A constante dos gases pode ser admitida como 8314kPa.cm3 .mol-1.K-1.

Fonte: Arquivo da Banca Elaboradora.
O fluxo de água que evapora é igual a
Um vaso fechado, a 120°C, contém 0,55mol de fenol e 0,45mol de tolueno. Nessa temperatura, a pressão de vapor do fenol é 13,0kPa e a do metanol é 131,3kPa.
Considerando que o sistema se encontra no ponto de orvalho, que a fase líquida se comporta como uma solução ideal e a fase vapor se comporta como uma mistura de gases ideais, a pressão no interior do vaso é
Um mol de gás, em um vaso fechado, passa por um ciclo termodinâmico de 4 etapas. Na tabela a seguir estão apresentadas as variações da energia interna do gás, o calor adicionado ao sistema e o trabalho realizado pelo sistema em algumas etapas em que foi possível realizar as medições (dados em branco não foram medidos).
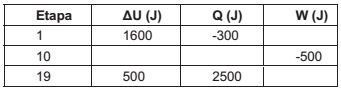
Fonte: Arquivo da Banca Elaboradora.
Na quadragésima etapa, foram adicionados 1300J ao sistema na forma de calor e o trabalho realizado pelo
sistema foi de
As equações a seguir são as relações termodinâmicas fundamentais para 1 mol de um fluido homogêneo com composição constante.
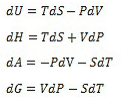
As propriedades termodinâmicas expressas nessas equações são: energia interna (U), entalpia (H), energia de Helmholtz (A), energia de Gibbs (G), temperatura (T), pressão (P), volume (V) e entropia (S).
A partir dessas relações fundamentais, é possível encontrar outras correlações que permitem realizar
experimentos simples para estudos bastante complexos. Por exemplo, caso queira verificar como a energia
de Gibbs varia com a entropia, mantendo-se a temperatura constante, pode-se utilizar os dados de um
experimento em que observa-se a variação da(o)
A seguir são apresentadas as entalpias de formação de alguns compostos. Analise-as
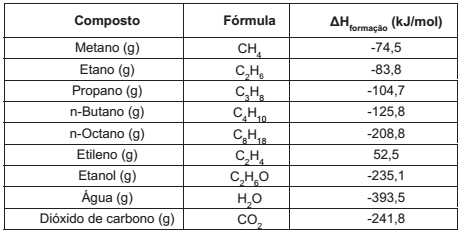
SMITH, J. M.; VAN NESS, H. C.; ABBOTT, M. M. Introdução à termodinâmica da Engenharia Química. 7 ed. Rio de Janeiro: LTC, 2007. p. 514-515.
A partir da análise desses dados, é correto afirmar que