Questões de Concurso Militar CIAAR 2019 para Primeiro Tenente - Engenharia Química
Foram encontradas 60 questões
Água deve ser bombeada a uma vazão de 1m3 .h, a partir de um reservatório para o topo de uma coluna de absorção, segundo o esquema representado a seguir. O reservatório é aberto e a pressão da água na entrada da coluna deve ser igua a 2 atm (P2 ).
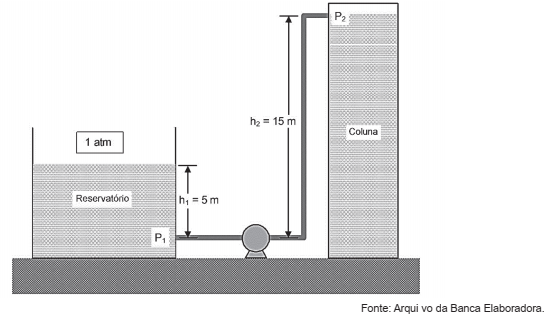
Considerando que a eficiência de operação da bomba é de 75% e que as perdas por atrito nas tubulações
podem ser desprezadas, a potência requerida pela bomba é
Quando um material sofre corrosão, é importante avaliar a composição desse material, o meio corrosivo e sob quais condições operacionais ele ficou exposto. De acordo com o tipo de material e o meio corrosivo, a corrosão pode ser química ou eletroquímica.
Associe corretamente o mecanismo de corrosão ao(s) respectivo(s) processo(s) de corrosão.
MECANISMOS DE CORROSÃO
(1) Químico
(2) Eletroquímico
PROCESSOS DE CORROSÃO
( ) Ataque da borracha por ozônio.
( ) Oxidação do ferro exposto ao ambiente.
( ) Ataque do aço inox pelo cloro, em presença de umidade.
( ) Oxidação do aço inox por O2, em ambiente seco, formando Cr2 O3
O escoamento de água, em fluxo turbulento, em uma tubulação de aço inoxidável AISI 304, com diâmetro de 6 polegadas com brusca redução para 3 polegadas, levou à deterioração do aço com a formação de pites pouco depois do ponto de redução do diâmetro da tubulação.
Com base no exposto, é correto afirmar que a tubulação sofreu corrosão por
Na figura a seguir, é apresentado o diagrama de equilíbrio para sistema SO2(g) – H2O(l), no qual é expressa a solubilidade do dióxido de enxofre na água como uma função da pressão do gás e da temperatura do sistema.
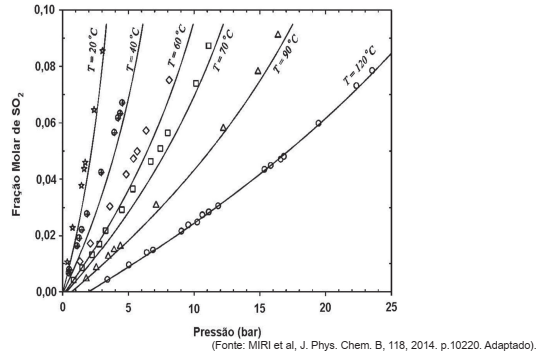
Com base nessa figura, avalie o que se afirma.
I. O aumento da pressão exercida pelo gás favorece a absorção do SO2 (g) pela água.
II. O aumento da temperatura aumenta a capacidade de absorção do SO2 (g) pelo solvente.
III. Na temperatura T = 20° , a absorção ocorre mais rapidamente que à temperatura T = 120° .
Está correto apenas o que se afirma em
O ácido acético pode ser produzido por meio da hidrólise do anidrido acético em fase líquida, conforme a seguinte reação.
(CH3CO)2O + H2O ⟶ 2 CH3COOH
A adsorção é um fenômeno de superfície no qual espécies em fase líquida ou gasosa, chamadas adsorvatos, ligam-se à superfície do adsorvente por meio de interações físicas, químicas ou ambas. Além da catálise heterogênea, a adsorção também é aplicada à purificação de gases e a o tratamento de efluentes líquidos, entre outros usos. Para determinar o grau de recobrimento da superfície do adsorvente, como uma função da concentração do adsorvato no meio líquido ou gasoso, à temperatura constante, são estabelecidas as isotermas de adsorção.
O processo de adsorção pode ser representado por meio da seguinte equação
A + S ⇌ AS
em que A é o adsorvato, no estado líquido ou gasoso, S representa o sítio vazio na superfície do adsorvente e AS representa o sítio ocupado por A na superfície do adsorvente.
A adsorção de ácido acético em carvão ativado pode ser descrita pela isoterma de Freundlich, expressa pela seguinte equação
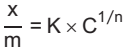
em que x é a massa de material adsorvido, m é a massa de material adsorvente, K e n são as constantes
do modelo e C é a concentração da solução (g.L-1) no equilíbrio. Os dados de equilíbrio para a adsorção de
ácido acético, a partir de soluções aquosas, em carvão ativado, são apresentados na figura a seguir.
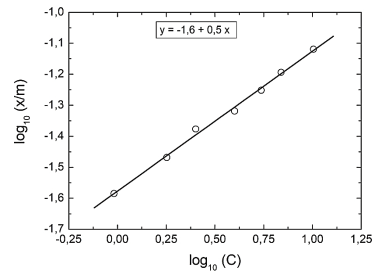
A partir dos dados apresentados no gráfico, é correto afimar que os valores das constantes K e n são,
respectivamente,
A reação elementar de segunda ordem, em fase líquida
2A → B
é conduzida isotermicamente, à 40° C, em um reator batelada de 100 dm3 . A constante de velocidade, na temperatura de operação do reator, é igual a 0,2 dm3 .mol-1.min-1. Cinquenta mols do reagente A são adicionados puros ao reator no início do processo.
O tempo necessário, em minutos, para que 50% de A seja consumido é igual a
Vapor de água escoa através de uma tubulação de aço, com 5m de comprimento, 20cm diâmetro interno e 5mm de espessura, a uma vazão de 1,0 kg.s-1. O vapor entra na tubulação saturado e sai 10% liquefeito, à pressão de 1atm, conforme indicado a seguir
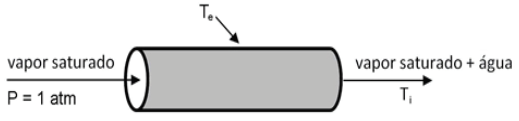
Dados adicionais:
k = 50 W.m-1. °C-1 (condutividade do aço)
HL = 419 kJ.kg-1 (entalpia específica do líquido saturado a 1atm)
HV = 2677 kJ.kg-1 (entalpia específica do vapor saturado a 1atm)
ln(re /ri ) = 0,025
A quantidade de calor transferida, por condução, através da tubulação é
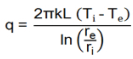
em que k é a condutividade térmica do aço, L é comprimento da tubulação, ri é o raio interno da tubulação e re é o raio externo, Ti e Te são as temperaturas interna e externa da tubulação, respectivamente.
A partir dos dados fornecidos, considerando-se desprezíveis as variações de energia cinética e de pressão,
pode-se dizer que a temperatura na parede externa da tubulação (Te) é
A síntese do trióxido de enxofre é um processo exotérmico

A dependência da constante de equilíbrio (Keq) com a temperatura é dada pela equação de van’t Hoff
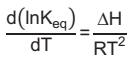
em que Keq é a constante de equilíbrio, ΔH é a entalpia da reação, R é a constante universal dos gases
(R = 8,3 J.mol-1.K-1) e T é a temperatura. Sabendo-se que Keq (300 K)=1 e considerando-se a entalpia da
reação aproximadamente constante nessa faixa de temperatura, o aumento da temperatura da reação de
20 °C desloca o equilíbrio da reação no sentido de formação dos
Um litro de uma solução de HCl com pH = 2 deve ser neutralizada com uma solução de NaOH 1 mol.L-1.
O volume, em mL, da solução básica necessário para realizar essa neutralização é igual a
O poli(metacrilato de metila) (PMMA), também conhecido como acrílico, é um polímero rígido transparente produzido a partir da polimerização do metacrilato de metila. O PMMA é um derivado do ácido metacrílico (CH2 =C[CH3 ]CO2 H), cuja estrutura do mero é a seguinte
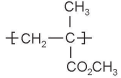
(Fonte: Enciclopédia Britânica. Disponível em: <https://www.britannica.com/science/ polymethyl-methacrylate> Acesso em: 17 fev. 2019.)
O PMMA é um material muito utilizado como substituinte do vidro. Ele é produzido na forma de chapas que podem ser usinadas ou moldadas por aquecimento, podendo também ser moldado por injeção.
Como base no exposto, é correto classificar o PMMA como um
A sim-trimetilenotrinitramina (C3 H6 N6 O6 ), também conhecida como RDX ou ciclonita, é um poderoso explosivo utilizado na fabricação de minas, cargas de profundidade e em torpedos, entre outros.
Sua estrutura química é apresentada a seguir.
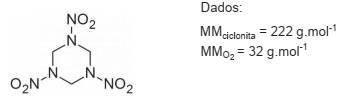
A detonação de um explosivo é uma reação de oxidação, provocada por impacto ou por ação do calor. Quando a quantidade de oxigênio presente na molécula do explosivo é insuficiente para que a oxidação completa ocorra, parte do oxigênio provém de fontes externas, como o ar atmosférico. O balanço de oxigênio para a molécula de explosivo fornece a fração de oxigênio, em percentual mássico, insuficiente ou excedente, que a molécula apresenta relativamente à quantidade necessária para a sua oxidação completa.
No caso da ciclonita, esse percentual é de
Considere a reação de queima do etanol
C2H5OH(l) + 3O2(g) →2CO2(g) + 3H2O(l) ΔcH (298 K; 1 bar) = -1368,0 kJ.mol-1
Se a combustão ocorre em recipiente exposto, à pressão atmosférica e as espécies gasosas se comportam
idealmente, a variação de energia interna por mol de etanol oxidado é
Uma central termoelétrica, capaz de gerar 50 MW de potência, opera a uma eficiência térmica máxima de 40%.
A taxa de energia dissipada para o ambiente é
No gráfico a seguir, são fornecidos dados da variação do coeficiente de correlação generalizada para o metano como uma função da pressão e da temperatura reduzidas.
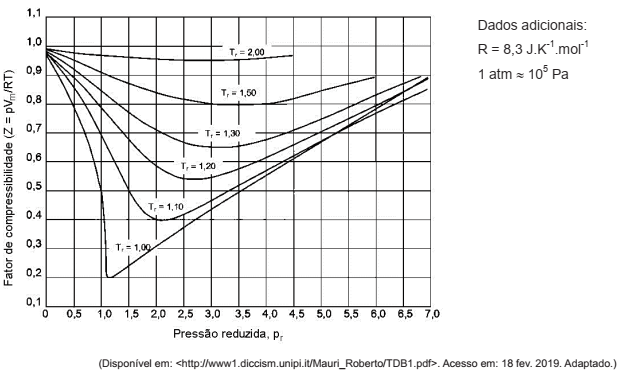
Sabendo-se que a pressão crítica do metano é pc = 45atm, a temperatura crítica é Tc = 190K e que a entalpia
de combustão do CH4
é igual a - 890kJ.mol-1, a vazão volumétrica com que o metano deve ser alimentado
na caldeira é igual a
As soluções-tampão são muito utilizadas em processos químicos e biológicos para efetuar o controle de pH.
Com relação a essas soluções, avalie as afirmativas a seguir.
I. Um exemplo de solução-tampão é aquela que contém uma base fraca e um sal derivado desta base fraca.
II. A solução-tampão resiste às variações de pH quando se adicionam pequenas quantidades de um ácido ou de uma base.
III. Adicionando-se quantidades equimolares de ácido acético e de hidróxido de sódio à água, obtém-se uma solução-tampão.
É correto apenas o que se afirma em
O cianeto de sódio (NaCN) é um sal usado principalmente na indústria de mineração para a recuperação de metais preciosos. É produzido industrialmente pela reação entre ácido cianídrico e hidróxido de sódio, sendo recuperado, após a sua purificação, na forma cristalina ou na forma de soluções contendo entre 27 e 32% m/m.
Sabendo-se que, à temperatura de 25°C, a constante de dissociação do NaCN em água é igual a Ka = 6,2x10-10, é correto afirmar que, para uma concentração igual a 6,25 mol.L-1 (~ 27% m/m), a solução é
O ácido etilenodiaminotetracético (EDTA), é um composto orgânico utilizado na indústria química e de cosméticos, além de ser muito utilizado em análises químicas por titulação complexométrica. Sua estrutura química é apresentada abaixo.
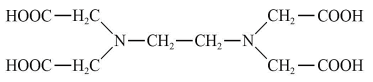
Com relação às reações de complexação, utilizando-se o ácido etilenodiaminotetracético, é correto afirmar
que o EDTA
A análise granulométrica de quatro tipos de materiais é aprentada a seguir, indicando a fração mássica acumulada de particulado fino passante em função do diâmetro da peneira.
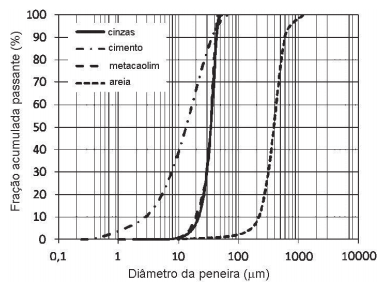
Fonte: LIMA et al., 2014. (Disponível em:<https://www.researchgate.net/figure/ Granulometric-analysis-of-materials_fig2_270566670> . Acesso em 19 fev. 2019. Adaptado).
Um particulado sólido, resultante da moagem de um material de composição desconhecida, apresenta a seguinte distribuição granulométrica diferencial.
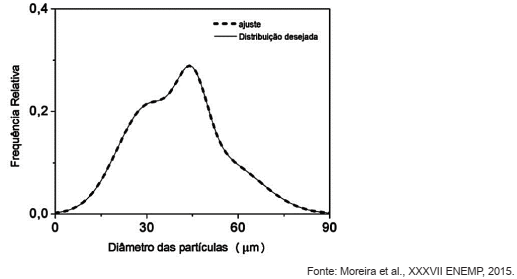
A esse respeito, avalie as afirmações a seguir.
I. 30% da mistura apresenta particulado com diâmetro de 45 µm.
II. Trata-se de uma mistura de, pelo menos, três componentes ou fases sólidas distintas.
III. Os diâmetros predominantes para cada componente ou fase sólida são da ordem de 30 µm, 45 µm e 60 µm.
IV. A área sob a curva fornece a massa total das partículas presentes no sistema com diâmetros entre 0 e 90 µm.
Está correto apenas o que se afirma em