Questões de Concurso Militar ITA 2019 para Aluno - Matemática, Física, Química, Português e Inglês
Foram encontradas 15 questões
I. O ácido tricloroacético é um ácido mais fraco que o ácido propanóico. II. O 2,4,6-tricloro-fenol possui um caráter ácido maior que o 2,4,6-trinitro-fenol. III. Reações de hidratação de alcinos geram produtos tautoméricos. IV. Anéis benzênicos sofrem reações de substituição pela interação com reagentes eletrófilos, enquanto haletos orgânicos sofrem substituição pela interação com reagentes nucleófilos.
Das afirmações acima, está(ão) CORRETA(S)
Anodo, H2 → 2H+ + 2e- (E° = 0 V) Catodo, Br2 + 2e- → 2Br- (E° = 1,087 V)
A dissociação da água pode ser observada pelo efeito da seguinte semirreação:
O2 + 4e-+ 4H+ → 2H2O E° = 1,229 V
A formação de complexos iônicos de polibrometo ocorre segundo as reações e suas respectivas constantes de equilíbrio:
Br2 + Br- ⇌ Br3- K3 = 16,7 2Br2 + Br- ⇌ Br5- K5 = 37,7
Sejam feitas as seguintes afirmações a respeito dessa bateria:
I. O potencial da célula pode ser aproximado pela equação: Ecatodo - Eanodo = 1,087 + 0,06 pH. II. O solvente (água) é termodinamicamente estável somente a pH < 2,4.
III. Recarregar a bateria com um potencial catódico inferior a 1,229 V garante a estabilidade do solvente. IV. Durante a descarga da bateria, a concentração do HBr aumenta e podem formar complexos ionicos de Br3- e Br5-.
Das afirmações acima, estão CORRETAS
I. O aumento da pressão no reator, mediante adição de um gás inerte, aumenta o rendimento do processo. II. O uso de um catalisador mais efetivo aumenta o rendimento do processo. III. Uma vez atingido o equilíbrio, não ocorrem mais colisões efetivas entre moléculas de H2(g) e N2(g). IV. Considerando que ainda exista superação da energia de ativação, a redução da temperatura no reator diminui a velocidade da reação, mas favorece a formação de amônia.
Assinale a opção que apresenta a(s) afirmação(ões) CORRETA(S) sobre a reação de formação da amônia.
I. A parafina da vela é constituída por moléculas de fórmula molecular CxHy, em que x < 8. II. A combustão da parafina na vela tem como principais produtos: negro de fumo, monóxido de carbono, dióxido de carbono e água. III. cor amarela da parte superior da chama indica um processo de combustão que depende da difusão do oxigênio presente no ar. IV. Na região inferior da chama há coloração levemente azulada por conta da maior quantidade de oxigênio difundido pelas zonas de recirculação.
Das afirmações acima, está(ão) CORRETA(S)
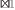 1, na solução resultante é igual a
1, na solução resultante é igual a (1) A glicose é um álcool-aldeído que polimeriza para formar o amido e a celulose. (2) A estrutura primária de um polipeptídeo é a sequência de resíduos de aminoácidos. (3) Os polímeros formados por cadeias longas tendem a ter alta viscosidade. (4) Os álcoois condensam com ácidos carboxílicos para formar ésteres. (5) As amidas resultam da condensação de aminas e ácidos carboxílicos.
A soma dos números associados às afirmativas CORRETAS é igual a:
I. Conversão de propanol em propanal; II. Conversão de bromometano em metanol; III. Conversão de etino em eteno; IV. Reação de propanal em presença de íons prata; V . Conversão de metano em bromometano.
As reações envolvidas em cada uma das transformações de I a V podem ser classificadas como de oxidação, redução, ou outra. Assinale a opção que contém corretamente o tipo de reação envolvida, do ponto de vista da molécula orgânica, em cada uma das transformações de I a V, respectivamente.
I. A uma solução de nitrato de prata é adicionada uma solução de cloreto de sódio, com a formação de um precipitado. II. O precipitado obtido em (I) é filtrado e misturado a hidróxido de sódio sólido, com um pouco de água. A mistura é aquecida, produzindo um sólido marrom escuro. III. O sólido preparado em (II) é aquecido junto a uma solução concentrada de glicose, formando um sólido cinzento.
Assinale a alternativa que apresenta corretamente os sólidos produzidos em I, II e III, respectivamente.