Questões de Concurso Militar EsPCEx 2017 para Cadete do Exército - 1° Dia
Foram encontradas 44 questões
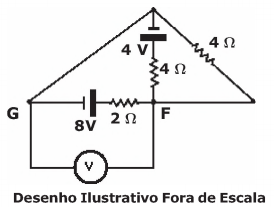
O desenho abaixo representa um circuito elétrico composto por gerador, receptor, condutores, um voltímetro (V), todos ideais, e resistores ôhmicos. O valor da diferença de potencial (ddp), entre os pontos F e G do circuito, medida pelo voltímetro, é igual a
Um bloco A de massa 100 kg sobe, em movimento retilíneo uniforme, um plano inclinado que forma um ângulo de 37° com a superfície horizontal. O bloco é puxado por um sistema de roldanas móveis e cordas, todas ideais, e coplanares. O sistema mantém as cordas paralelas ao plano inclinado enquanto é aplicada a força de intensidade F na extremidade livre da corda, conforme o desenho abaixo.
Todas as cordas possuem uma de suas extremidades fixadas em um poste que permanece imóvel quando as cordas são tracionadas.
Sabendo que o coeficiente de atrito dinâmico entre o bloco A e o plano inclinado é de 0,50,
a intensidade da força 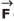 é
é
Dados: sen 37° = 0,60 e cos 37° = 0,80
Considere a aceleração da gravidade igual a 10 m/s2.
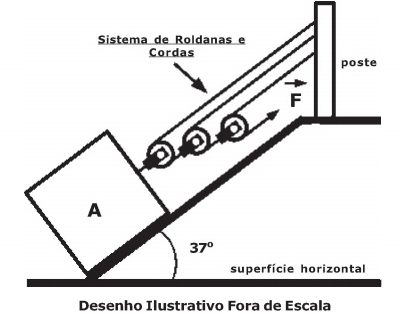
Uma haste AB rígida, homogênea com 4 m de comprimento e 20 N de peso, encontra-se
apoiada no ponto C de uma parede vertical, de altura 1,5  √3 m, formando um ângulo de 30º com
ela, conforme representado nos desenhos abaixo.
√3 m, formando um ângulo de 30º com
ela, conforme representado nos desenhos abaixo.
Para evitar o escorregamento da haste, um cabo horizontal ideal encontra-se fixo à extremidade da barra no ponto B e a outra extremidade do cabo, fixa à parede vertical.
Desprezando todas as forças de atrito e considerando que a haste encontra-se em equilíbrio estático, a força de tração no cabo é igual a
Dados: sen 30° = cos 60° = 0,5 e sen 60° = cos 30° = √3/2
Uma granada de mão, inicialmente em repouso, explode sobre uma mesa indestrutível, de superfície horizontal e sem atrito, e fragmenta-se em três pedaços de massas m1, m2 e m3 que adquirem velocidades coplanares entre si e paralelas ao plano da mesa.
Os valores das massas são m1 = m2= m e m3 = m/2 . Imediatamente após a explosão, as massas m1 e m2 adquirem as velocidades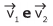 , respectivamente, cujos módulos são iguais a v, conforme
o desenho abaixo.
Desprezando todas as forças externas, o módulo da velocidade
, respectivamente, cujos módulos são iguais a v, conforme
o desenho abaixo.
Desprezando todas as forças externas, o módulo da velocidade 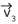 , imediatamente após a
explosão é
, imediatamente após a
explosão é 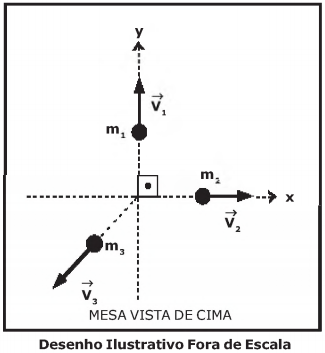
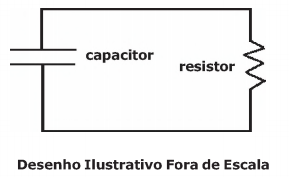
Um capacitor de capacitância igual a 2 μF está completamente carregado e possui uma diferença de potencial entre suas armaduras de 3 V. Em seguida, este capacitor é ligado a um resistor ôhmico por meio de fios condutores ideais, conforme representado no circuito abaixo, sendo completamente descarregado através do resistor.
Nesta situação, a energia elétrica total transformada em calor pelo resistor é de
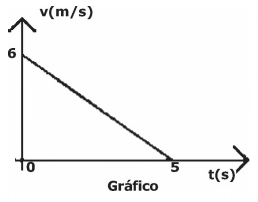
Um bloco de massa igual a 1,5 kg é lançado sobre uma superfície horizontal plana com atrito com uma velocidade inicial de 6 m/s em t1= 0 s. Ele percorre uma certa distância, numa trajetória retilínea, até parar completamente em t2=5 s, conforme o gráfico abaixo.
O valor absoluto do trabalho realizado pela força de atrito sobre o bloco é
Um painel coletor de energia solar é utilizado para aquecer a água de uma residência e todo o sistema tem um rendimento de 60%. Para aumentar a temperatura em 12,0 °C de uma massa de água de 1000 kg, a energia solar total coletada no painel deve ser de
Dado: considere o calor específico da água igual a 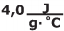 .
.
Uma partícula com carga elétrica negativa igual a -10-8 C encontra-se fixa num ponto do espaço. Uma segunda partícula de massa igual a 0,1 g e carga elétrica positiva igual a +10-8 C descreve um movimento circular uniforme de raio 10 cm em torno da primeira partícula. Considerando que elas estejam isoladas no vácuo e desprezando todas as interações gravitacionais, o módulo da velocidade linear da partícula positiva em torno da partícula negativa é igual a
Dado: considere a constante eletrostática do vácuo igual a 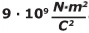 .
.
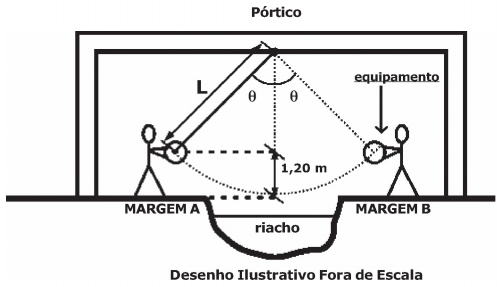
Um operário, na margem A de um riacho, quer enviar um equipamento de peso 500 N para outro operário na margem B.
Para isso ele utiliza uma corda ideal de comprimento L=3m, em que uma das extremidades está amarrada ao equipamento e a outra a um pórtico rígido.
Na margem A, a corda forma um ângulo θ com a perpendicular ao ponto de fixação no pórtico. O equipamento é abandonado do repouso a uma altura de 1,20 m em relação ao ponto mais baixo da sua trajetória. Em seguida, ele entra em movimento e descreve um arco de circunferência, conforme o desenho abaixo e chega à margem B.
Desprezando todas as forças de atrito e considerando o equipamento uma partícula, o módulo da força de tração na corda no ponto mais baixo da trajetória é
Dado: considere a aceleração da gravidade g=10 m/s2
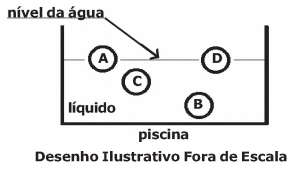
Quatro objetos esféricos A, B, C e D, sendo respectivamente suas massas mA, mB, mC e mD, tendo as seguintes relações mA>mB e mB = mC = mD, são lançados dentro de uma piscina contendo um líquido de densidade homogênea. Após algum tempo, os objetos ficam em equilíbrio estático. Os objetos A e D mantêm metade de seus volumes submersos e os objetos C e B ficam totalmente submersos conforme o desenho abaixo.
Sendo VA, VB, VC e VD os volumes dos objetos A, B, C e D, respectivamente, podemos afirmar que
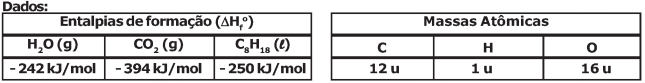
Algumas viaturas militares administrativas possuem motores à combustão que utilizam como combustível a gasolina. A queima (combustão) de combustíveis como a gasolina, nos motores à combustão, fornece a energia essencial para o funcionamento dessas viaturas militares. Considerando uma gasolina na condição padrão (25 °C e 1 atm), composta apenas por n-octano (C8H18) e que a sua combustão seja completa (formação exclusiva de CO2 e H2O gasosos como produtos), são feitas as seguintes afirmativas:
I - a combustão da gasolina (C8H18) é uma reação exotérmica;
II - na combustão completa de 1 mol de gasolina, são liberados 16 mols de gás carbônico (CO2);
III - a entalpia de combustão (calor de combustão) dessa gasolina é - 5080 kJ/mol (ΔHc=-5080 kJ/mol);
IV - o calor liberado na combustão de 57 g de gasolina é de 1270 kJ.
Das afirmativas apresentadas estão corretas apenas a
A emissão de gases derivados do enxofre, como o dióxido de enxofre (SO2), pode ocasionar uma série de problemas ambientais e a destruição de materiais como rochas e monumentos à base de calcita (carbonato de cálcio). Essa destruição ocasiona reações com a emissão de outros gases, como o gás carbônico (CO2), potencializando o efeito poluente. Considerando as equações das reações sucessivas a 27 °C e 1 atm, admitindo-se os gases como ideais e as reações completas, o volume de CO2 produzido a partir da utilização de 2 toneladas de SO2 como reagente é, aproximadamente,
Dados
Massas Atômicas: S = 32 u ; O = 16 u ; H = 1 u ; C = 12 u ; Ca = 40 u
Constante dos gases ideais: R = 0,082 atm L
L mol-1
mol-1 K-1
K-1
Volume molar nas condições em que ocorreu a reação (27° e 1 atm) = 24,6 L/mol
SO2 (g) + 1/2 O2 (g) → SO3 (g) (equação I)
SO3 (g) + H2O (ℓ) → H2SO4 (ℓ) (equação II)
H2SO4 (ℓ) + CaCO3 (s) → CaSO4 (s) + H2O (ℓ) + CO2 (g) (equação III)
A gasolina é um combustível constituído por uma mistura de diversos compostos químicos, principalmente hidrocarbonetos. Estes compostos apresentam volatilidade elevada e geram facilmente vapores inflamáveis.
Em um motor automotivo, a mistura de ar e vapores inflamáveis de gasolina é comprimida por um pistão dentro de um cilindro e posteriormente sofre ignição por uma centelha elétrica (faísca) produzida pela vela do motor.
Adaptado de: BROWN, Theodore; L. LEMAY, H Eugene; BURSTEN, Bruce E. Química a Ciência Central, 9ª edição, Editora Prentice-Hall, 2005, pág 926.
Pode-se afirmar que a centelha elétrica produzida pela vela do veículo neste evento tem a
função química de
Conversores catalíticos (catalisadores) de automóveis são utilizados para reduzir a emissão de poluentes tóxicos. Poluentes de elevada toxicidade são convertidos a compostos menos tóxicos. Nesses conversores, os gases resultantes da combustão no motor e o ar passam por substâncias catalisadoras. Essas substâncias aceleram, por exemplo, a conversão de monóxido de carbono (CO) em dióxido de carbono (CO2) e a decomposição de óxidos de nitrogênio como o NO, N2O e o NO2 (denominados NOx) em gás nitrogênio (N2) e gás oxigênio (O2). Referente às substâncias citadas no texto e às características de catalisadores, são feitas as seguintes afirmativas:
I - a decomposição catalítica de óxidos de nitrogênio produzindo o gás oxigênio e o gás nitrogênio é classificada como uma reação de oxidorredução;
II - o CO2 é um óxido ácido que, ao reagir com água, forma o ácido carbônico;
III - catalisadores são substâncias que iniciam as reações químicas que seriam impossíveis sem eles, aumentando a velocidade e também a energia de ativação da reação;
IV - o CO é um óxido básico que, ao reagir com água, forma uma base;
V - a molécula do gás carbônico (CO2) apresenta geometria espacial angular.
Das afirmativas feitas estão corretas apenas a
"Sempre que uma substância muda de fase de agregação, a temperatura permanece constante enquanto a mudança se processa, desde que a pressão permaneça constante".
FONSECA Martha Reis Marques da, Química Geral, São Paulo: Ed FTD, 2007, pág 41.
O gráfico abaixo representa a mudança de fase de agregação de uma substância pura com o passar do tempo, em função da variação de temperatura, observada ao se aquecer uma substância X durante algum tempo, sob pressão constante.
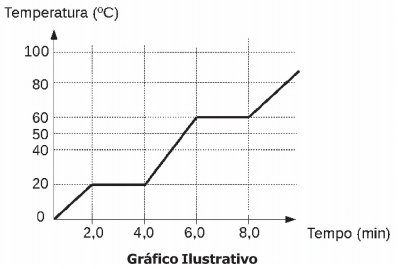
Tomando-se como base o gráfico, analise as seguintes afirmativas:
I - entre 0 °C e 19 °C, a substância X encontra-se na fase sólida;
II - o intervalo de 2,0 min a 4,0 min corresponde à condensação da substância X;
III - a temperatura de 60 °C corresponde à temperatura de ebulição da substância X;
IV - no intervalo de 40 °C a 50 °C, a substância X encontra-se na fase líquida.
Estão corretas apenas as afirmativas
Quando um átomo, ou um grupo de átomos, perde a neutralidade elétrica, passa a ser denominado de íon. Sendo assim, o íon é formado quando o átomo (ou grupo de átomos) ganha ou perde elétrons. Logicamente, esse fato interfere na distribuição eletrônica da espécie química. Todavia, várias espécies químicas podem possuir a mesma distribuição eletrônica.
Considere as espécies químicas listadas na tabela a seguir:

A distribuição eletrônica 1s2, 2s2, 2p6, 3s2, 3p6 (segundo o Diagrama de Linus Pauling) pode
corresponder, apenas, à distribuição eletrônica das espécies
Na ânsia pelo "elixir da longa vida", por volta do século I, alquimistas descobriram acidentalmente a Pólvora, referenciada em textos de Alquimia pelos avisos quanto aos cuidados para não se misturarem certos materiais uns com os outros. A pólvora, mais conhecida desde o final do século XIX como pólvora negra, é uma mistura química que queima com rapidez. Foi extensamente utilizada como propelente em canhões e armas de fogo e atualmente ainda é empregada em artefatos pirotécnicos. Nitrato de potássio, enxofre e carvão (carbono) são os constituintes da pólvora negra. Sobre as espécies constituintes da pólvora negra afirma-se que
Dados:
Número Atômico: K = 19; N = 7; O = 8; S = 16; C = 6
I - o nitrato de potássio é classificado como uma base segundo a teoria de Arrhenius;
II - a 25 °C e 1 atm a variedade alotrópica mais estável do carbono é a grafite e a do enxofre é a rômbica;
III - a fórmula do nitrato de potássio é KNO2 ;
IV - o enxofre é um metal radioativo que pertence à família 6A (16) da tabela periódica;
V - o átomo de carbono (6C) estabelece 4 ligações químicas e possui a variedade alotrópica diamante, substância natural de alta dureza;
Estão corretas apenas as afirmativas
O polímero Kevlar® (poliparafenileno de tereftalamida), usado em materiais de proteção balística, foi descoberto pela química sueca Stephanie Kwolek, na tentativa de desenvolver um novo polímero para uso em pneus. Apresenta elevada resistência térmica e mecânica por suas cadeias estabelecerem uma rede polimérica, por meio de interações intermoleculares fortes. Pode ser sintetizado a partir da reação entre as substâncias 1,4-fenileno-diamina (1,4 - diaminobenzeno) e ácido tereftálico (ácido 1,4 - benzenodicarboxílico) como mostra a equação da reação a seguir:
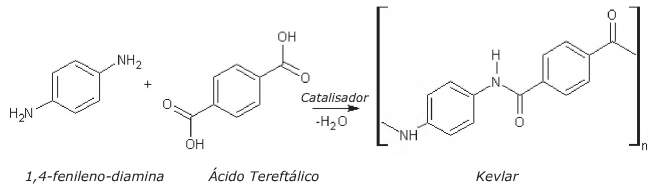
Com relação a esta reação e às estruturas apresentadas, são feitas as seguintes afirmativas:
I - a hibridização de todos os carbonos nas estruturas dos reagentes é do tipo sp2;
II - a reação de obtenção do poliparafenileno de tereftalamida é classificada como de substituição, por adicionar uma molécula de água à estrutura do polímero;
III - o Kevlar é uma substância iônica de alta massa molecular;
IV - a fórmula molecular da substância 1,4-fenileno-diamina é C6H8N2;
V - as interações intermoleculares que mantêm as cadeias do Kevlar unidas, formando redes poliméricas, são do tipo ligações de hidrogênio (pontes de hidrogênio).
Estão corretas apenas as afirmativas