Questões de Concurso Militar CAP 2018 para Cabo - Técnico em Química
Foram encontradas 50 questões
O decaimento do trício, um isótopo radioativo do hidrogênio empregado em pesquisas com reatores nucleares de fusão e em armas termonucleares, está representado no gráfico a seguir.
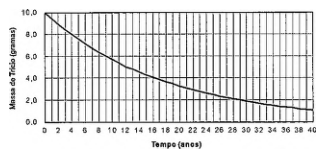
Uma amostra de trício apresenta uma atividade radioativa inicial de 3,0x109 desintegrações por segundo. Com base nos dados e no gráfico acima, pode-se prever que essa amostra apresentará uma atividade de 7,5x108 desintegrações por segundo após, aproximadamente:
Dados:
In(2) = 0,69 ln(3) = 1,1 ln(4) = 1,4
In (6) = 1,8 ln(7,5) = 2,0
Observe os compostos abaixo.
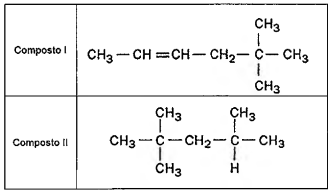
Assinale a opção que apresenta o nome (IUPAC) para os
compostos I e II, respectivamente.
O tratamento quantitativo da absorção de energia radiante pela matéria depende do princípio geral conhecido como Lei de Beer, a qual se encontra abaixo representada:
A = a.b.c, onde
A = Absorbância, a = absortividade, b = caminho óptico da amostra, c = concentração do absorvente.
Em relação à Lei de Beer e seus parâmetros, é correto afirmar que:
Coloque F (falso) ou V (verdadeiro) nas afirmativas abaixo, em relação às técnicas básicas para análises em laboratório, assinalando a seguir a opção correta.
( ) As laterais da câmara de pesagem da balança analítica de prato único não precisam ser fechadas, tendo em vista que a medição nesse tipo de equipamento não é afetada por correntes de ar externo.
( ) A calcinação de precipitados é feita em cadinhos de porcelana, em atmosfera oxidante e de maneira bem lenta, de forma que não haja nenhuma mudança química do precipitado causada pelo carbono proveniente da queima do papel-filtro.
( ) A calibração é o processo para medir a quantidade real de uma grandeza que corresponde à quantidade indicada na escala de um instrumento.
( ) Durante o processo de limpeza, um aparelho volumétrico deve ser aquecido para remoção de gorduras e impurezas porventura contidas nas suas paredes internas, haja vista que esses equipamentos não deformam durante o procedimento.
( ) A água-régia, substância empregada no preparo de soluções em gravimetria, é utilizada para a solubilização de metais.
Observe a tabela abaixo:

O valor da entalpia-padrão de combustão do benzeno liquido a partir das entalpias de formação dos reagentes e produtos da reação, conforme tabela acima, considerando uma combustão completa, é:
Dado: reação de combustão do benzeno:
C6H6 (l) + 15/2 O2(g) → 6CO2(g) + 3H2O(I)
Um técnico em química observou o desprendimento de um gás numa reação química em laboratório e coletou uma amostra para análise. Ao medir a densidade do gás a 25°C e 1,0 atm, ele encontrou o valor de 2,38 g/dm3. Além disso, constatou que o referido gás era composto de 80% de carbono e 20% de hidrogênio em massa. Sendo assim, qual é a fórmula empírica e massa molar do composto gasoso analisado, respectivamente, assumindo que o gás obedece a lei dos gases ideais?
Dados: R = 0,082 atm L mol-1 K-1
A preparação de superfície é, sem dúvida, uma das etapas mais importantes para que um revestimento apresente o desempenho esperado. Com relação à preparação de superfície para pintura, avalie as afirmativas abaixo.
I- O hidrojateamento é um método de preparação de superfície bastante utilizado no campo da pintura anticorrosiva e tem, entre outras, as seguintes características técnicas: é eficiente na remoção de contaminantes, especialmente sais solúveis; não gera pó nem produz faíscas durante a operação de limpeza; e confere rugosidade à superfície.
II- Na preparação de superfície, são removidos os contaminantes da superfície, assim como são criadas condições que proporcionam aderência satisfatória aos revestimentos.
III- A limpeza por solventes é uma etapa fundamental, pois visa a remover completamente os contaminantes oleosos e os produtos de corrosão da superfície.
Assinale a opção correta.
O módulo de descida lunar da Apoio utilizou a dimetil-hidrazina (CH3)2NNH2 como combustível juntamente com o N2O4 líquido como oxidante. A reação química entre os dois reagentes no motor do foguete ocorre conforme descrito na equação química balanceada a seguir:
(CH3)2NNH2 + 2N2O4 → 4H2O + 2CO2 + 3N2
Analise o seguinte equilíbrio:

Suponha que o valor da constante de equilíbrio é 300 a
600 K, e que a concentração das quatro espécies inicia-se
a 0,100 mol/L. Assinale a opção que apresenta de que
maneira essas concentrações mudarão, à medida que o
sistema se aproxima do equilíbrio, se a temperatura for
mantida a 600 K.
As seguintes velocidades iniciais foram obtidas como dados experimentais para uma reação hipotética 2A + B → C + 3D:

Considerando os dados acima, qual é a equação de
velocidade da reação e o valor da constante de
velocidade, respectivamente?
Observe a reação a seguir:
HCI(aq) + NaOH(aq) → NaCI(aq) + H2O(I)
Assinale a opção que completa corretamente as lacunas da sentença abaixo:
O cloreto de prata é menos solúvel em uma solução de NaCI do que em água pura. Nesse caso, a redução de solubilidade pode ser explicada pelo fenômeno denominado_______, baseado no_________.