Questões de Concurso Militar EsFCEx 2020 para Oficial - Magistério de Química
Foram encontradas 30 questões
A figura representa a curva de aquecimento de uma substância.
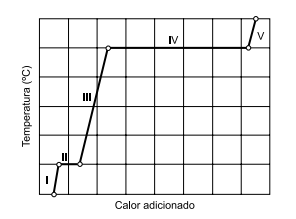
(Brown, T. L.; Lemay Jr, H. E.; Bursten, B. E.; Burdge, J. R.
Química, a ciência central. Adaptado)
As regiões da curva em que a substância se encontra em
dois estados físicos são:
Esse experimento refere-se___________ e à emissão de______________ .
Assinale a alternativa que completa, correta e respectivamente, as lacunas.
Considere os seguintes pares de compostos iônicos:
I. MgO e MgS.
II. KBr e CaBr2 .
III. MgF2
e CaF2.
Os compostos que apresentam maior energia reticular
em I, II e III, são, correta e respectivamente,
Assinale a alternativa que completa, correta e respectivamente, as lacunas.
Considere as substâncias I, II, III e IV cujas fórmulas estruturais são representadas nas figuras.
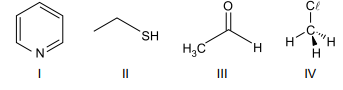
Formam interações intermoleculares do tipo ligação de
hidrogênio com a água as substâncias
A substância AyXz é um sólido cristalino e sua célula unitária é representada na figura.
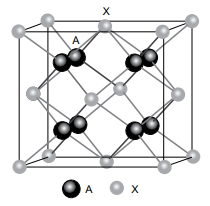
(Morozova, N. V. et al. Journal of Applied Physics. Adaptado)
A fórmula unitária da substância AyXz é
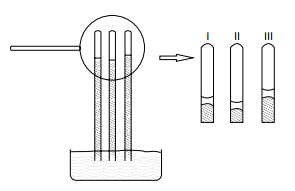
Nesse experimento, a água, a solução de cloreto de sódio e a solução de glicose estão contidas, respectivamente, nos tubos
Considere os dados apresentados na tabela.

(Bottecchia, O.L. Química Nova. Adaptado)
Considerando que a massa molar do ar em toda a atmosfera é aproximadamente constante, 29 g.mol–1
, o valor
da pressão atmosférica na mesosfera, X, na temperatura
indicada na tabela é aproximadamente
Completou-se o volume do balão com água destilada. Considerando que se empregou a técnica quantitativa na preparação da solução, a concentração de íons nitrato na solução preparada é
Considere a curva de solubilidade da sacarose.
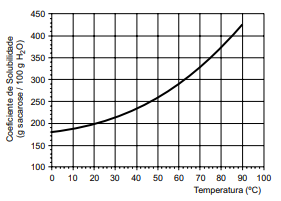
A temperatura em que se iniciou a cristalização e a massa máxima de açúcar cristalizada na solução em repouso a 20 ºC são, correta e respectivamente,
Considerando que a reação cessa após o consumo total do reagente limitante, ao serem misturados 12 mol de cada um dos reagentes, a quantidade máxima de fosfeto de boro que pode ser formada e a quantidade total de reagentes que permanecem sem reagir são, respectivamente,
CaC2O4 (s) ➝ CaCO3 (s) + CO (g) CaCO3 (s) ➝ CaO (s) + CO2 (g)
O resultado da análise é apresentado na forma de uma curva da variação de massa em função da temperatura ao longo do processo de aquecimento.
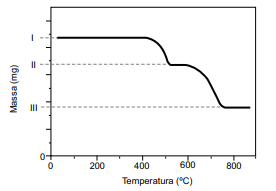
(Cavalheir, E. T. G.; et al. Química Nova. Adaptado)
I. 51,2 mg da amostra da mistura de CaC2 O4 e SiO2 . II. 42,8 mg. III. 29,6 mg.
O teor de oxalato de cálcio nessa amostra é de
I. NH4+ + NH2 – ➝ 2NH3 . II. CH3 NH2 + H2O ➝ CH3 NH3+ + OH– III. SO3 2– + S ➝ S2 O3 2–
As espécies que atuam como ácido nas reações representadas em I, II e III são, respectivamente,
2 Na+(eletrólito) + 2 e– ➝ 2 Na(l) Eº = –2,71 V S8 (l) + 16 e– ➝ 8 S2– (eletrólito) Eº = –0,51 V
O potencial padrão dessa bateria e o número de elétrons transferidos para cada molécula S8 (l), são, respectivamente,
Considerando a constante de Faraday 9,65 x 104 C.mol–1 , a massa máxima de níquel e ouro depositadas nesse período de funcionamento do sistema foi, respectivamente, de, aproximadamente,

As melhores condições para que a formação do produto seja favorecida são:
Considere a tabela dos valores de Kw a diferentes temperaturas.
T (ºC) Kw
10 0,29 × 10–14
15 0,45 × 10–14
20 0,68 × 10–14
25 1,01 × 10–14
30 1,47 × 10–14
50 5,48 × 10–14
Os valores de Kw mostram que, a 50 ºC, o pH da água
pura é
