Questões Militares
Foram encontradas 455 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
 . L-1. Para obtenção da concentração final nessa diluição, o
volume de água destilada que deve ser adicionado é de
. L-1. Para obtenção da concentração final nessa diluição, o
volume de água destilada que deve ser adicionado é de
Células galvânicas (pilhas) são dispositivos nos quais reações espontâneas de oxidorredução geram uma corrente elétrica. São dispostas pela combinação de espécies químicas com potenciais de redução diferentes. Existem milhares de células galvânicas possíveis. Considere as semirreações abaixo e seus respectivos potenciais de redução nas condições padrão (25 °C e 1 atm).
Al3+ (aq) + 3 e- → Al (s) ΔE°red = -1,66 V
Au3+ (aq) + 3 e- → Au (s) ΔE°red = +1,50 V
Cu2+ (aq) + 2 e- → Cu (s) ΔE°red = +0,34 V
Baseado nas possibilidades de combinações de células galvânicas e suas representações esquemáticas recomendadas pela União Internacional de Química Pura e Aplicada (IUPAC), são feitas as seguintes afirmativas:
I - a diferença de potencial (d.d.p.) da pilha formada pelas espécies químicas alumínio e cobre e representada esquematicamente por Al(s)|Al3+(aq)||Cu2+ (aq) |Cu (s) é de +1,52 V (nas condições-padrão);
II - na pilha formada pelas espécies químicas cobre e ouro e representada esquematicamente por Cu (s) |Cu2+(aq) || Au3+(aq) |Au (s), a reação global corretamente balanceada é:
3 Cu (s) + 2 Au3+ (aq) → 3 Cu2+ (aq) + 2 Au (s)
III - na pilha formada pelas espécies químicas cobre e ouro e representada esquematicamente por Cu (s) | Cu2+(aq) || Au3+ (aq) | Au (s), o agente redutor é o Cu (s);
IV - a representação IUPAC correta de uma pilha de alumínio e ouro (Al-Au) é Au (s) | Au3+(aq) || Al3+(aq) | Al (s).
Estão corretas apenas as afirmativas
O trioxano, cuja fórmula estrutural plana simplificada encontra-se representada a seguir, é utilizado em alguns países como combustível sólido para o aquecimento de alimentos armazenados em embalagens especiais e que fazem parte das rações operacionais militares.
Considere a reação de combustão completa de um tablete de 90 g do trioxano com a formação de CO2 e H2O. Baseado nas energias de ligação fornecidas na tabela abaixo, o valor da entalpia de combustão estimada para esta reação é
Dados:
Massas Atômicas: O=16 u ; H = 1 u ; C=12 u.

O polímero Kevlar® (poliparafenileno de tereftalamida), usado em materiais de proteção balística, foi descoberto pela química sueca Stephanie Kwolek, na tentativa de desenvolver um novo polímero para uso em pneus. Apresenta elevada resistência térmica e mecânica por suas cadeias estabelecerem uma rede polimérica, por meio de interações intermoleculares fortes. Pode ser sintetizado a partir da reação entre as substâncias 1,4-fenileno-diamina (1,4 - diaminobenzeno) e ácido tereftálico (ácido 1,4 - benzenodicarboxílico) como mostra a equação da reação a seguir:
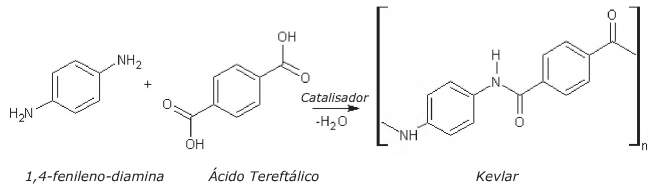
Com relação a esta reação e às estruturas apresentadas, são feitas as seguintes afirmativas:
I - a hibridização de todos os carbonos nas estruturas dos reagentes é do tipo sp2;
II - a reação de obtenção do poliparafenileno de tereftalamida é classificada como de substituição, por adicionar uma molécula de água à estrutura do polímero;
III - o Kevlar é uma substância iônica de alta massa molecular;
IV - a fórmula molecular da substância 1,4-fenileno-diamina é C6H8N2;
V - as interações intermoleculares que mantêm as cadeias do Kevlar unidas, formando redes poliméricas, são do tipo ligações de hidrogênio (pontes de hidrogênio).
Estão corretas apenas as afirmativas
Na ânsia pelo "elixir da longa vida", por volta do século I, alquimistas descobriram acidentalmente a Pólvora, referenciada em textos de Alquimia pelos avisos quanto aos cuidados para não se misturarem certos materiais uns com os outros. A pólvora, mais conhecida desde o final do século XIX como pólvora negra, é uma mistura química que queima com rapidez. Foi extensamente utilizada como propelente em canhões e armas de fogo e atualmente ainda é empregada em artefatos pirotécnicos. Nitrato de potássio, enxofre e carvão (carbono) são os constituintes da pólvora negra. Sobre as espécies constituintes da pólvora negra afirma-se que
Dados:
Número Atômico: K = 19; N = 7; O = 8; S = 16; C = 6
I - o nitrato de potássio é classificado como uma base segundo a teoria de Arrhenius;
II - a 25 °C e 1 atm a variedade alotrópica mais estável do carbono é a grafite e a do enxofre é a rômbica;
III - a fórmula do nitrato de potássio é KNO2 ;
IV - o enxofre é um metal radioativo que pertence à família 6A (16) da tabela periódica;
V - o átomo de carbono (6C) estabelece 4 ligações químicas e possui a variedade alotrópica diamante, substância natural de alta dureza;
Estão corretas apenas as afirmativas