Questões Militares
Para exército
Foram encontradas 21.017 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Considere as informações abaixo para responder a questão.
A seguir são apresentados os potências padrão de redução para algumas semirreações:

I. Ferro sólido colocado em solução de Sn 2+ (aq) não reagirá.
II. Solução de cobre(II) pode ser conservada em tonéis de estanho.
III. No eletrodo padrão de hidrogênio o pH é igual a zero.
IV. Uma pilha com eletrodo de cobre em solução de Cu 2+ (aq) 0,5 mol/l e estanho em solução de Sn 2+ (aq) 0,5 mol/l, apresenta 0,48 V de f.e.m.
Considere a equação abaixo para responder a questão.

Considere a equação abaixo para responder a questão.

I. o composto (a) é o ácido conjugado da piridina.
II. o composto (a) é base mais forte que (b) e (c).
III. os grupos metil aumentam a força básica da piridina.
IV. o composto (b) é um ácido mais fraco que (c).
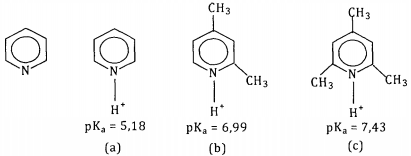
Das informações dadas estão corretas:
( ) Espécies químicas que têm na sua composição hidrogênio com carga parcial positiva, Hδ+, são ácidos de Arrhenius.
( ) Bases de Brönsted-Lowry têm na sua composição átomos com pares de elétrons não-ligantes.
( ) Bases de Brönsted-Lowry, em água, produzem íons OH-.
( ) Ácidos de Arrhenius são substâncias iônicas.
I. Segundo o princípio de Le Châtelier a adição de H+ ao sistema tampão faz liberar mesma quantidade de OH-.
II. O sistema tampão funciona no sistema digestivo, mas não no sistema sanguíneo.
III. Por adição do sal à solução do ácido para formar o tampão, a percentagem de dissociação do ácido diminui.
IV. A solução tampão sofre pequena variação de pH quando a ela são adicionados íons H+ ou OH-.
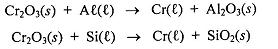
Após balancear as equações acima, assinale a alternativa correta.
I. Ambas as etapas 1 e 2 ocorrem com absorção de calor.
II. Se a energia da etapa 3 suplantar a soma de 1 e 2, o processo é exotérmico.
III. A etapa 3 pode ser exotérmica ou endotérmica a depender do soluto.
IV. Se a soma de 1 e 2 for maior que o módulo de 3, a dissolução libera calor.
V. Se a energia para separar as partículas do soluto for elevada, não ocorrerá a dissolução.
I. A fusão do enxofre elementar,S8(s) produz moléculas S8
II. Sílica, (SiO2)n é um exemplo de sólido molecular.
III. A fusão da sílica, (SiO2)n, ocorre com quebra das ligações Si-O.
IV. Sólidos iônicos são bons condutores de eletricidade.
V. As partículas formadoras dos sólidos metálicos são átomos.
I. A molécula I2 é mais polarizável que Cl2
II. O momento de dipolo de HI é maior que o de HCl.
III. O cátion Na+ é mais polarizante que Li+
IV. O caráter covalente no cloreto de lítio é maior que no cloreto de sódio.
V. As forças intermoleculares entre Cl2 são mais intensas que entre I2-
PF5. SF4, SF6, SO42-, NO2, HCN, BF4-
Com relação a essas espécies pode-se afirmar que:
O esquema a seguir representa de um modo geral, o diagrama de energia para os orbitais moleculares de moléculas diatômicas formadas por elementos do 2° período da tabela periódica.
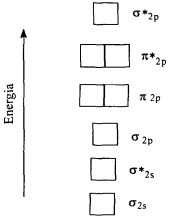
Ao usá-lo para fazer as configurações eletrônicas das espécies químicas N2, O2,
0 2+, F2, e CO, pode-se afirmar que: