Questões Militares Comentadas por alunos sobre termoquímica: energia calorífica, calor de reação, entalpia, equações e lei de hess. em química
Foram encontradas 66 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Dados: massas atômicas: C = 12 u ; O = 16 u ; H = 1 u
4C(S) + S8(S) → 4 CS2(1) ΔH = + 358,8 kJ
Se o calor absorvido durante a reação foi de 3588 kj, quantos mols de CS2 foram produzidos?
2NO (g) + O2(g),→ 2NO2(g) ΔH = ?
Qual o valor da entalpia padrão da reação acima?
Dados:
N2(g) + O2(g) → 2NO(g) ΔH = +180,5 kJ
N2(g) + 2O2(g) → 2NO2(g) ΔH = + 66,4 kJ
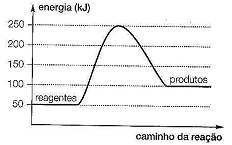
Considerando o gráfico anterior, referente ao diagrama energético de uma reação química, qual o valor da energia de ativação e o ΔH da reação respectivamente?
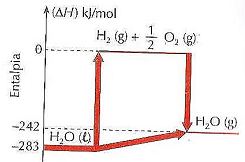
A partir do diagrama de entalpia, marque V para as afirmativas verdadeiras e F para as falsas.
( ) A quantidade de calor envolvido na decomposição de 126 g de H2O(l) → H2(g) + ½ O2(g) é 1.981 kJ/mol.
( ) H2O(l) → H2O(g) ΔH = –41 kJ/mol.
( ) H2(g) + ½ O2(g)→ H2O(g) ΔH = +242 kJ/mol.
A sequência está correta em
