Questões Militares
Foram encontradas 266 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
A proteção catódica é uma técnica de combate à corrosão, usada como complementar à ação protetora dos revestimentos que, por melhores e mais bem aplicados que sejam, sempre contêm falhas e poros e se tornam deficientes com o tempo. Para a obtenção da proteção catódica, dois sistemas são utilizados, ambos baseados no princípio de injeção de corrente elétrica na estrutura: proteção catódica galvânica e a proteção catódica por corrente impressa. Considerando a necessidade de instalação de anodos de zinco em uma estrutura metálica revestida e submersa em água do mar, calcule a corrente elétrica necessária para sua proteção catódica, em A (Àmpere), sabendo que a estrutura de 100 m2 está pintada com um revestimento de eficiência média igual a 90% e que se movimenta em relação à água do mar a uma velocidade de 3 m/s, e assinale a opção correta.
Dados: densidade de corrente elétrica da água do mar = 55 mA/m2.

Observe a tabela abaixo:

O valor da entalpia-padrão de combustão do benzeno liquido a partir das entalpias de formação dos reagentes e produtos da reação, conforme tabela acima, considerando uma combustão completa, é:
Dado: reação de combustão do benzeno:
C6H6 (l) + 15/2 O2(g) → 6CO2(g) + 3H2O(I)
O decaimento do trício, um isótopo radioativo do hidrogênio empregado em pesquisas com reatores nucleares de fusão e em armas termonucleares, está representado no gráfico a seguir.
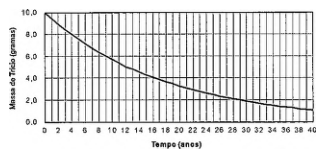
Uma amostra de trício apresenta uma atividade radioativa inicial de 3,0x109 desintegrações por segundo. Com base nos dados e no gráfico acima, pode-se prever que essa amostra apresentará uma atividade de 7,5x108 desintegrações por segundo após, aproximadamente:
Dados:
In(2) = 0,69 ln(3) = 1,1 ln(4) = 1,4
In (6) = 1,8 ln(7,5) = 2,0
O calorímetro é utilizado no laboratório para inúmeros propósitos, incluindo a determinação da energia produzida na queima de combustíveis e o conteúdo calórico dos alimentos. Numa bomba calorimétrica, assume-se que a quantidade de calor absorvido (ou liberado) pela combinação de água, o interior do calorímetro, a bomba e a mistura reagente seja igual à produzida (ou absorvida) pela reação que ocorre na bomba. Considerando que uma amostra de 0,728 g de etanol (álcool de cereais, C2H5OH) é queimada numa bomba calorimétrica com uma quantidade de gás oxigênio (sob pressão) suficiente para assegurar a combustão completa, qual é o calor molar de combustão do etanol, sabendo que, nesse experimento, a quantidade de água no calorímetro é de 1,20 kg e que a temperatura aumenta de 24,86°C para 29,18°C?
Dados: capacidade calorífica do interior do calorímetro (sem água) é de 1,06 kJ °C-1 e a capacidade calorífica molar da água é 75,3 J °C-1 mol-1.