Questões Militares
Foram encontradas 456 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
O composto mais comum de cálcio é o carbonato de cálcio, que ocorre naturalmente na forma de calcário. O calcário é decomposto por aquecimento em óxido de cálcio e dióxido de carbono. Por sua vez, o óxido de cálcio reage exotermicamente com a água, formando o hidróxido de cálcio, conhecido como cal apagado.
Assinale a alternativa que apresenta corretamente as fórmulas químicas dos compostos citados no texto: carbonato de cálcio, óxido de cálcio, dióxido de carbono e hidróxido de cálcio:
Em processos industriais, a dureza elevada da água pode ser prejudicial, pois há tendência à incrustação de sais nas caldeiras, principalmente quando a água é aquecida. O aquecimento da água converte todo bicarbonato presente em carbonato pela eliminação de dióxido de carbono.
Ca(HCO3 )2(aq) → Xs + CO2(g) + H2O
A letra X representa qual sal?
O etanol, utilizado como combustível em carros flex, é produzido pelo processo de fermentação, do caldo de cana, “garapa”, onde leveduras transformam a sacarose em álcool, segundo a reação simplificada:
C12H22O11 + H2O → 2C6H12O6
C6H12O6 → CH3CH2OH + 2CO2 ∆H = -23,5kcal
A fermentação da sacarose trata-se de um processo:
Nestes últimos anos, os alunos da EsPCEx têm realizado uma prática no laboratório de química envolvendo eletrólise com eletrodos inertes de grafite. Eles seguem um procedimento experimental conforme a descrição:
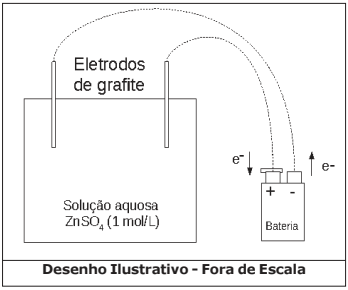
- Num béquer de capacidade 100 mL (cuba eletrolítica) coloque cerca de 50 mL de solução aquosa de sulfato de zinco (ZnSO4) de concentração 1 mol·L-1. Tome como eletrodos duas barras finas de grafite. Ligue-as com auxílio de fios a uma fonte externa de eletricidade (bateria) com corrente de 2 Ampères. Esta fonte tem capacidade para efetuar perfeitamente esse processo de eletrólise. Uma das barras deve ser ligada ao polo negativo da fonte e a outra barra ao polo positivo da fonte. Mergulhe os eletrodos na solução durante 32 minutos e 10 segundos e observe.
Considere o arranjo eletrolítico (a 25 ºC e 1 atm), conforme visto na figura a seguir:
Dados: 1 Faraday (F) = 96500 Coulomb (C) / mol de elétrons
Acerca do experimento e os conceitos químicos envolvidos são feitas as seguintes afirmativas:
I – Na superfície da barra de grafite ligada como cátodo da eletrólise ocorre a eletrodeposição do zinco metálico.
II – A semirreação de oxidação que ocorre no ânodo da eletrólise é Zn (s) → Zn2+ (aq) + 2 e- .
III – Durante o processo a barra de grafite ligada ao polo positivo da bateria se oxida.
IV – No ânodo da eletrólise ocorre uma reação de oxidação da hidroxila com formação do gás oxigênio e água.
V – A massa de zinco metálico obtida no processo de eletrólise será de 0,83 g.
Das afirmativas feitas, estão corretas apenas