Questões Militares
Foram encontradas 106 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Considerando-se que a primeira ionização do H2SO4 seja praticamente completa e a segunda, parcial, é correto concluir que o pH da água do lago, após a contaminação pelo ácido, atinge valor inferior a 4,0.
Caso o acidente em questão tenha ocorrido em um dia frio, com a temperatura da água a 5 ºC, é correto concluir que, no instante imediatamente anterior ao derramamento, o pH da água do lago era superior a 7,0.
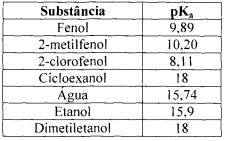
Com base nos valores apresentados no quadro, assinale a alternativa correta.
I. Segundo o princípio de Le Châtelier a adição de H+ ao sistema tampão faz liberar mesma quantidade de OH-.
II. O sistema tampão funciona no sistema digestivo, mas não no sistema sanguíneo.
III. Por adição do sal à solução do ácido para formar o tampão, a percentagem de dissociação do ácido diminui.
IV. A solução tampão sofre pequena variação de pH quando a ela são adicionados íons H+ ou OH-.
Dados: Kw = 10-14 (mol · L-1)2
