Questões Militares
Foram encontradas 342 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
O decaimento do trício, um isótopo radioativo do hidrogênio empregado em pesquisas com reatores nucleares de fusão e em armas termonucleares, está representado no gráfico a seguir.
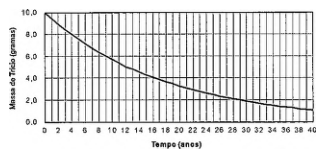
Uma amostra de trício apresenta uma atividade radioativa inicial de 3,0x109 desintegrações por segundo. Com base nos dados e no gráfico acima, pode-se prever que essa amostra apresentará uma atividade de 7,5x108 desintegrações por segundo após, aproximadamente:
Dados:
In(2) = 0,69 ln(3) = 1,1 ln(4) = 1,4
In (6) = 1,8 ln(7,5) = 2,0
O hidróxido de magnésio é praticamente insolúvel na ausência de sais de amônio e tem um produto de solubilidade de 3,2x10-11 à temperatura ambiente. A dissociação desse hidróxido é representada por:
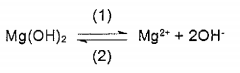
Calcule a concentração de íons hidroxila, em mol.L-1, em
uma solução aquosa saturada, e assinale a opção
correspondente.
O calorímetro é utilizado no laboratório para inúmeros propósitos, incluindo a determinação da energia produzida na queima de combustíveis e o conteúdo calórico dos alimentos. Numa bomba calorimétrica, assume-se que a quantidade de calor absorvido (ou liberado) pela combinação de água, o interior do calorímetro, a bomba e a mistura reagente seja igual à produzida (ou absorvida) pela reação que ocorre na bomba. Considerando que uma amostra de 0,728 g de etanol (álcool de cereais, C2H5OH) é queimada numa bomba calorimétrica com uma quantidade de gás oxigênio (sob pressão) suficiente para assegurar a combustão completa, qual é o calor molar de combustão do etanol, sabendo que, nesse experimento, a quantidade de água no calorímetro é de 1,20 kg e que a temperatura aumenta de 24,86°C para 29,18°C?
Dados: capacidade calorífica do interior do calorímetro (sem água) é de 1,06 kJ °C-1 e a capacidade calorífica molar da água é 75,3 J °C-1 mol-1.
Constantes de equilíbrio de ácidos fracos a 25 oC

Com base nas informações fornecidas, qual dos sais indicados a seguir é o mais eficiente como solução neutralizante?
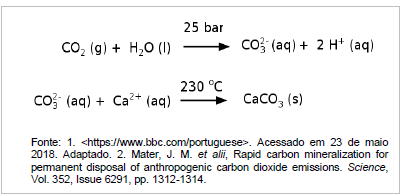
A remoção desse gás da atmosfera ocorre por: