Questões Militares
Foram encontradas 320 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Células galvânicas (pilhas) são dispositivos nos quais reações espontâneas de oxidorredução geram uma corrente elétrica. São dispostas pela combinação de espécies químicas com potenciais de redução diferentes. Existem milhares de células galvânicas possíveis. Considere as semirreações abaixo e seus respectivos potenciais de redução nas condições padrão (25 °C e 1 atm).
Al3+ (aq) + 3 e- → Al (s) ΔE°red = -1,66 V
Au3+ (aq) + 3 e- → Au (s) ΔE°red = +1,50 V
Cu2+ (aq) + 2 e- → Cu (s) ΔE°red = +0,34 V
Baseado nas possibilidades de combinações de células galvânicas e suas representações esquemáticas recomendadas pela União Internacional de Química Pura e Aplicada (IUPAC), são feitas as seguintes afirmativas:
I - a diferença de potencial (d.d.p.) da pilha formada pelas espécies químicas alumínio e cobre e representada esquematicamente por Al(s)|Al3+(aq)||Cu2+ (aq) |Cu (s) é de +1,52 V (nas condições-padrão);
II - na pilha formada pelas espécies químicas cobre e ouro e representada esquematicamente por Cu (s) |Cu2+(aq) || Au3+(aq) |Au (s), a reação global corretamente balanceada é:
3 Cu (s) + 2 Au3+ (aq) → 3 Cu2+ (aq) + 2 Au (s)
III - na pilha formada pelas espécies químicas cobre e ouro e representada esquematicamente por Cu (s) | Cu2+(aq) || Au3+ (aq) | Au (s), o agente redutor é o Cu (s);
IV - a representação IUPAC correta de uma pilha de alumínio e ouro (Al-Au) é Au (s) | Au3+(aq) || Al3+(aq) | Al (s).
Estão corretas apenas as afirmativas
O trioxano, cuja fórmula estrutural plana simplificada encontra-se representada a seguir, é utilizado em alguns países como combustível sólido para o aquecimento de alimentos armazenados em embalagens especiais e que fazem parte das rações operacionais militares.
Considere a reação de combustão completa de um tablete de 90 g do trioxano com a formação de CO2 e H2O. Baseado nas energias de ligação fornecidas na tabela abaixo, o valor da entalpia de combustão estimada para esta reação é
Dados:
Massas Atômicas: O=16 u ; H = 1 u ; C=12 u.

Conversores catalíticos (catalisadores) de automóveis são utilizados para reduzir a emissão de poluentes tóxicos. Poluentes de elevada toxicidade são convertidos a compostos menos tóxicos. Nesses conversores, os gases resultantes da combustão no motor e o ar passam por substâncias catalisadoras. Essas substâncias aceleram, por exemplo, a conversão de monóxido de carbono (CO) em dióxido de carbono (CO2) e a decomposição de óxidos de nitrogênio como o NO, N2O e o NO2 (denominados NOx) em gás nitrogênio (N2) e gás oxigênio (O2). Referente às substâncias citadas no texto e às características de catalisadores, são feitas as seguintes afirmativas:
I - a decomposição catalítica de óxidos de nitrogênio produzindo o gás oxigênio e o gás nitrogênio é classificada como uma reação de oxidorredução;
II - o CO2 é um óxido ácido que, ao reagir com água, forma o ácido carbônico;
III - catalisadores são substâncias que iniciam as reações químicas que seriam impossíveis sem eles, aumentando a velocidade e também a energia de ativação da reação;
IV - o CO é um óxido básico que, ao reagir com água, forma uma base;
V - a molécula do gás carbônico (CO2) apresenta geometria espacial angular.
Das afirmativas feitas estão corretas apenas a
A gasolina é um combustível constituído por uma mistura de diversos compostos químicos, principalmente hidrocarbonetos. Estes compostos apresentam volatilidade elevada e geram facilmente vapores inflamáveis.
Em um motor automotivo, a mistura de ar e vapores inflamáveis de gasolina é comprimida por um pistão dentro de um cilindro e posteriormente sofre ignição por uma centelha elétrica (faísca) produzida pela vela do motor.
Adaptado de: BROWN, Theodore; L. LEMAY, H Eugene; BURSTEN, Bruce E. Química a Ciência Central, 9ª edição, Editora Prentice-Hall, 2005, pág 926.
Pode-se afirmar que a centelha elétrica produzida pela vela do veículo neste evento tem a
função química de
Algumas viaturas militares administrativas possuem motores à combustão que utilizam como combustível a gasolina. A queima (combustão) de combustíveis como a gasolina, nos motores à combustão, fornece a energia essencial para o funcionamento dessas viaturas militares. Considerando uma gasolina na condição padrão (25 °C e 1 atm), composta apenas por n-octano (C8H18) e que a sua combustão seja completa (formação exclusiva de CO2 e H2O gasosos como produtos), são feitas as seguintes afirmativas:
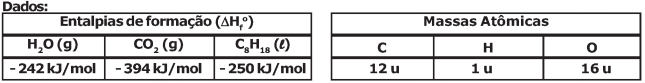
I - a combustão da gasolina (C8H18) é uma reação exotérmica;
II - na combustão completa de 1 mol de gasolina, são liberados 16 mols de gás carbônico (CO2);
III - a entalpia de combustão (calor de combustão) dessa gasolina é - 5080 kJ/mol (ΔHc=-5080 kJ/mol);
IV - o calor liberado na combustão de 57 g de gasolina é de 1270 kJ.
Das afirmativas apresentadas estão corretas apenas a