Questões Militares
Foram encontradas 487 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Considere os seguintes pares de compostos iônicos:
I. MgO e MgS.
II. KBr e CaBr2 .
III. MgF2
e CaF2.
Os compostos que apresentam maior energia reticular
em I, II e III, são, correta e respectivamente,
A figura representa a curva de aquecimento de uma substância.
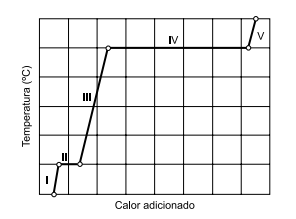
(Brown, T. L.; Lemay Jr, H. E.; Bursten, B. E.; Burdge, J. R.
Química, a ciência central. Adaptado)
As regiões da curva em que a substância se encontra em
dois estados físicos são:
No trecho “Quando estou com a água, não guardo mágoa. Explodo de emoção”, o autor descreve a maneira altamente energética com que sódio metálico reage com água, conforme equação a seguir:
a Na(s) + b H2O(l) c NaOH(aq) + d H2(g)
Na equação balanceada, os valores dos coeficientes estequiométricos a, b, c e d são, respectivamente:
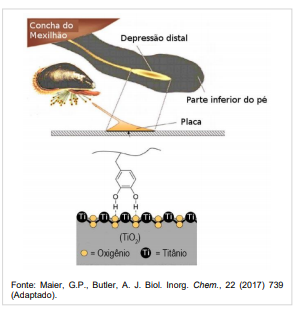
Os mexilhões aderem fortemente às rochas através de uma matriz de placas adesivas que são secretadas pela depressão distal localizada na parte inferior do seu pé. Essas placas adesivas são ricas em proteínas, as quais possuem em abundância o aminoácido LDopa. Esse aminoácido possui, em sua cadeia lateral, um grupo catechol (dihidroxibenzeno), que tem papel essencial na adesão do mexilhão à superfície rochosa. A figura ilustra um esquema da placa adesiva do mexilhão e um esquema da principal interação entre o grupo catechol e a superfície do óxido de titânio, que representa uma superfície rochosa.
A adesão do mexilhão à rocha deve-se principalmente à interação intermolecular do tipo:
O ânion perxenato (XeO6 4- ) é um oxidante muito forte, capaz de oxidar Mn(II) a Mn(VII), conforme a equação química abaixo:
5 Na4XeO6(aq) + 8 MnSO4(aq) + 2 H2O(l) → 5 Xe(g) + 8 NaMnO4(aq) + 6 Na2SO4(aq) + 2 H2SO4(aq)
Além disso, o XeO6 4- é um oxidante limpo, pois não introduz produtos de redução no meio da reação, uma vez que o xenônio formado está na forma de gás.
Um experimento foi realizado na temperatura de 300 K e 100 kPa, em que 16 mol de MnSO4 foram totalmente oxidados por Na4XeO6 e todo o gás produzido foi coletado. Nessas condições, o volume de um mol de um gás ideal é igual a 24,9 L.
O volume (em L) de gás coletado nesse experimento foi igual a:

