Questões Militares
Foram encontradas 532 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Em processos industriais, a dureza elevada da água pode ser prejudicial, pois há tendência à incrustação de sais nas caldeiras, principalmente quando a água é aquecida. O aquecimento da água converte todo bicarbonato presente em carbonato pela eliminação de dióxido de carbono.
Ca(HCO3 )2(aq) → Xs + CO2(g) + H2O
A letra X representa qual sal?
Algumas bactérias do solo, como as nitrobactérias, catalisam a oxidação do nitrogênio contido em sais de amônio (fertilizante químico) formando nitrato, o qual pode ser assimilado pelos vegetais.
2O2 + NH4+ → NO3- + 2H+ + H2O
É correto afirmar que o nitrogênio presente no
ânion nitrato apresenta um número de oxidação
(Nox) de:
Diagramas de fases são gráficos construídos para indicar uma condição de temperatura e pressão de uma substância e suas mudanças de estado. Cada uma das curvas do diagrama indica as condições de temperatura e pressão nas quais as duas fases de estado estão em equilíbrio.
Modificado de USBERCO, João e SALVADOR, Edgard, Físico-química, São Paulo, Ed Saraiva, 2009, Pág. 98
Considere o diagrama de fases da água, representado na figura abaixo:
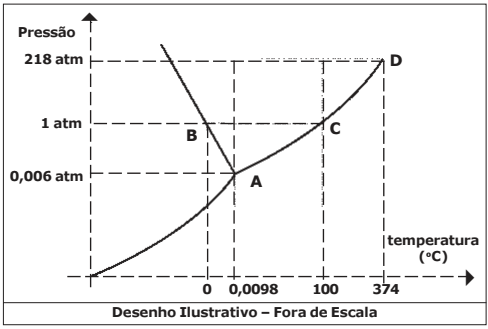
Baseado no diagrama e nos processos químicos envolvidos são feitas as seguintes afirmativas:
I – A temperatura de fusão da água aumenta com o aumento da pressão.
II – Na temperatura de 100 ºC e 218 atm a água é líquida.
III – A água sólida (gelo) sublima a uma pressão de vapor superior a 1 atm.
IV – Na temperatura de 0 ºC e pressão de 0,006 atm, a água encontra-se na fase sólida.
Das afirmativas feitas, estão corretas apenas
“No fenômeno físico, a composição da matéria é preservada, ou seja, permanece a mesma antes e depois da ocorrência do fenômeno”.
“Reação química é toda transformação que modifica a natureza da matéria (fenômenos químicos)”.
“No fenômeno químico, a composição da matéria é alterada: sua composição antes de ocorrer o fenômeno é diferente da que resulta no final”.
FONSECA, Martha Reis Marques da, Química Geral, São Paulo, Ed FTD, 2007, Pág. 24 e 61.
Considere os conceitos supracitados e as transformações representadas pelas equações químicas a seguir:
I – CaCO3 (s) → CaO (s) + CO2 (g)
II – H2O (l) →H2O (g)
III – H2 (g) + O2 (g) → H2O (g)
IV – C(grafite) + O2 (g) → CO2 (g)
Correspondem a reações químicas apenas as transformações
“Solução saturada: solução que contém a quantidade máxima de soluto em determinada quantidade de solvente, a determinada temperatura; a relação entre quantidades máximas de soluto e quantidade de solvente é denominada de coeficiente de solubilidade”.
“Solução insaturada: quando a solução contém uma quantidade de soluto inferior ao seu coeficiente de solubilidade, na temperatura em que se encontra a solução”.
“Solução supersaturada: quando a solução contém uma quantidade de soluto dissolvido superior ao seu coeficiente de solubilidade, na temperatura em que se ela se encontra. É instável” .
USBERCO, João e SALVADOR, Edgard, Físico-química, São Paulo, Ed Saraiva, 2009, Pág. 18
FONSECA, Martha Reis Marques da, Química Geral, São Paulo, Ed FTD, 2007, Pág. 18 e 19.
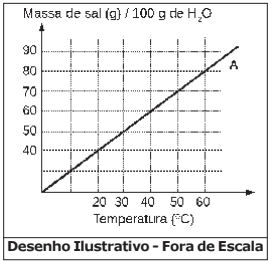
Considere o gráfico da curva de solubilidade em função da temperatura para um sal hipotético A. No gráfico, a linha contínua representa a solubilidade máxima do soluto (sal A) em 100 g de água na temperatura correspondente.
Acerca desse gráfico e processo de solubilidade são feitas as seguintes afirmativas:
I – Na temperatura de 20 ºC, misturando-se 50 g do sal A em 100 g de água, ter-se-á um sistema heterogêneo.
II – Na temperatura de 40 ºC, a adição de 50 g do sal A em 100 g de água produzirá uma solução insaturada.
III – 200 g de água dissolvem totalmente 90 g do sal A a 30 ºC.
IV – Uma solução contendo 60 g do sal A em 100 g de água será saturada em 60 ºC.
Das afirmativas feitas estão corretas apenas