Questões Militares
Foram encontradas 780 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Com os uniformes cobertos de barro, os militares bombeiros estavam por todos os lados no mar de lama e detritos que arrasou a cidade de Brumadinho devido ao acidente da barragem ocorrido no ano de 2019. A lama de rejeito provocou um rastro de destruição ao longo do Rio Paraopeba. Segundo especialistas, em toda a extensão percorrida, a água do rio não tinha condições para o consumo humano e animal. Dentre vários contaminantes, encontraram-se metais em altas concentrações como ferro, cobre, manganês e cromo.
Sobre os metais citados no texto, aquele que, quando o átomo se encontra ionizado no estado de oxidação +2 apresentará a configuração eletrônica 1s2 2s2 2p6 3s2 3p6 3d5 é o:
CAMPOS, B. Instituto Geral de Perícias de Santa Catarina. Disponível em: <https://www.sc.gov.br/noticias/temas/defesa civil-e-bombeiros/perito-do-igp-explica-semelhancas-entreexplosao -em-beirute-e-incidente-em-sao-francisco-do-sul>. Acesso em: 20 ago. 2020 (Adaptação).
Considerando que 20 toneladas do fertilizante com 65%m/m em nitrato de amônio foram expostas ao acidente e todo o nitrato foi queimado, qual é a massa mais próxima, em toneladas, de nitrogênio, detonada na explosão?
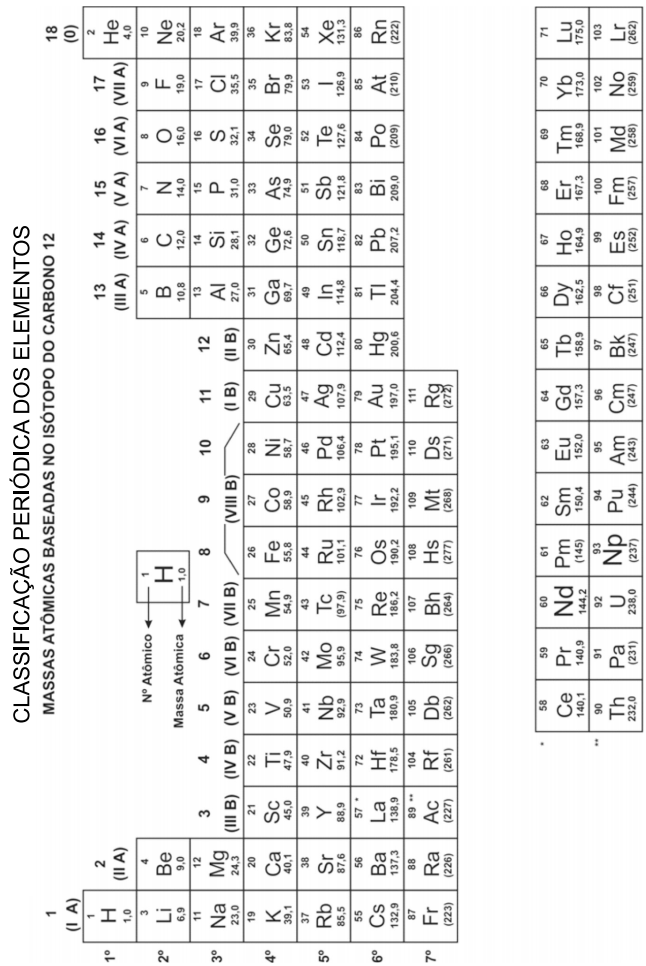
Em 2019, é comemorado o aniversário de 150 anos da primeira versão da tabela periódica, proposta por Dmitri Mendeleev. Ele criou um sistema que, além de catalogar os elementos, permitiu prever propriedades em função da posição que o elemento ocupa na tabela. Em 1869, o sódio (Na) e o potássio (K) já constavam da primeira versão da tabela periódica. Na versão atual, esses elementos pertencem ao primeiro grupo, o dos metais alcalinos. Esses metais reagem de maneira violenta com água, na qual se produz gás hidrogênio, conforme esquematizado abaixo:
2 M (s) + 2 H2O (l) → 2 MOH (aq) + H2(g), M = Na ou K
A propriedade comum a esse grupo, que é responsável pelo comportamento descrito em água, é o:
O ânion perxenato (XeO64- ) é um oxidante muito forte, capaz de oxidar Mn(II) a Mn(VII), conforme a equação química abaixo:
5 Na4XeO6(aq) + 8 MnSO4(aq) + 2 H2O(l) → 5 Xe(g) + 8 NaMnO4(aq) + 6 Na2SO4(aq) + 2 H2SO4(aq)
Além disso, o XeO64- é um oxidante limpo, pois não introduz produtos de redução no meio da reação, uma vez que o xenônio formado está na forma de gás.
Um experimento foi realizado na temperatura de 300 K e 100 kPa, em que 16 mol de MnSO4 foram totalmente oxidados por Na4XeO6 e todo o gás produzido foi coletado. Nessas condições, o volume de um mol de um gás ideal é igual a 24,9 L.
O volume (em L) de gás coletado nesse experimento foi igual a:
Num laboratório, um grupo de alunos possui quatro semicélulas montadas, todas em condição padrão de concentração e temperatura, correspondentes às semirreações mostradas no quadro abaixo:
Semicélula Semirreação de redução E0 / V
I MnO2 + 4H+ + 2e- → Mn2+ + 2H2O 1,23
II I2 + 2e- → 2I- 0,54
III Cu2+ + 2e- → Cu 0,34
IV Zn2+ + 2e- → Zn -0,76
Numa dada combinação para montar uma pilha eletroquímica, o valor de diferença de potencial (ΔE) da pilha, no instante em que se ligaram os contatos, foi de 0,69 V.
A combinação utilizada nessa pilha foi entre as semicélulas: