Questões Militares
Foram encontradas 514 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
A combustão completa do eicosano, um dos componentes da parafina utilizada para formar velas, é representada pela seguinte equação, não balanceada:
___ C20H42 + ___ O2 → ___ CO2 + ___H2O
Nessa equação, quando o coeficiente estequiométrico do
eicosano for 2, o do oxigênio será

O indicador vermelho de fenol apresenta cor amarela em
soluções aquosas de pH < 6,4, e, cor vermelha, em soluções
aquosas de pH > 8,2. Na água pura (pH = 7,0), esse indicador
apresenta cor laranja.
A uma amostra de água pura foi acrescentado o indicador vermelho de fenol. Em seguida, foi acrescentado certo óxido que mudou a cor apresentada por esse indicador de laranja para amarela. Esse óxido pode ter sido o
Considere as figuras I e II abaixo.
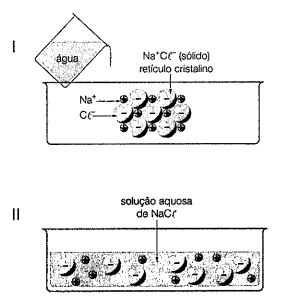
O fenômeno ocorrido na sequência I - II é denominado:
Considere as seguintes equações de neutralização.
H2SO4 + 2 NaOH → X + 2 H2O
H2SO4 + NaOH → Y + H2O
As substâncias que correspondem às letras X e Y são, respectivamente:
O cianeto de sódio (NaCN) é um sal usado principalmente na indústria de mineração para a recuperação de metais preciosos. É produzido industrialmente pela reação entre ácido cianídrico e hidróxido de sódio, sendo recuperado, após a sua purificação, na forma cristalina ou na forma de soluções contendo entre 27 e 32% m/m.
Sabendo-se que, à temperatura de 25°C, a constante de dissociação do NaCN em água é igual a Ka = 6,2x10-10, é correto afirmar que, para uma concentração igual a 6,25 mol.L-1 (~ 27% m/m), a solução é