Questões Militares
Foram encontradas 294 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Observe a figura a seguir.
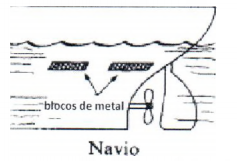
Para proteger da corrosão os cascos de navios, que são constituídos basicamente de ferro, é comum utilizarem-se blocos de um metal acoplados ao casco, conhecidos como metais de sacrifício, conforme representado na figura acima.
Dados:
Potenciais Padrão de Redução:
Fe2+ + 2e ↔ Fe E° = -0,44V
Cu2+ + 2e ↔ Cu E° = +0,34V
Zn2- + 2e ↔ Zn E° = -0,76V
Ni2+ + 2e ↔ Ni E° = -0,25V
Ag+ + e ↔ Ag E° = +0,79V
Pb2+ + 2e ↔ Pb E° = -0,13V
Utilizando os valores de potenciais acima relacionados, qual
é o metal de sacrifício que oferecerá melhor proteção ao
casco do os valores do navio?
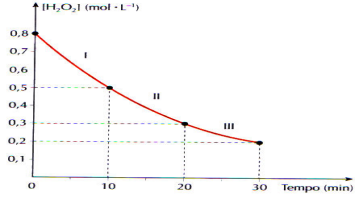 Calcule a velocidade média de decomposição da água
oxigenada, em mol.L-1.min-1, nos intervalos I, II, I e no
intervalo de 0 a 30 min:
Calcule a velocidade média de decomposição da água
oxigenada, em mol.L-1.min-1, nos intervalos I, II, I e no
intervalo de 0 a 30 min: 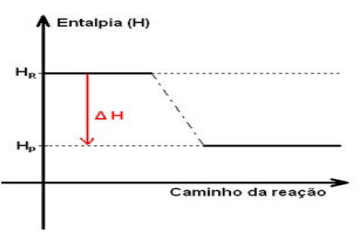
De acordo com o gráfico acima pode concluir se que trata se de uma reação Hp = 250, Hr = 480: I - Espontânea. II - Exotérmica, pois ocorreu um ganho de energia. III - Necessita apenas de um estímulo para que ocorra. IV - Sendo o Hp = 250 kj e Hr = 480kj o delta será de +130 kj. V - Endotérmica, pois ocorreu uma perda de energia. VI - Sendo o Hp = 250 e Hr = 480 delta H será de -130kj. Estão incorretas:
Considere duas reações químicas, mantidas à temperatura e pressão ambientes, descritas pelas equações abaixo:
I. H2(g) + 1/2 O2(g) → H2O(g)
ΙΙ. H2(g) + 1/2O2(g) → H2O(l )
Assinale a opção que apresenta a afirmação ERRADA sobre estas reações.
Considere o seguinte mecanismo de reação genérica:
A4++ B2+ → A3+ + B3+ (etapa lenta)
A4+ + B3+ → A3+ + B4+ (etapa rápida)
C+ + B4+ → C3+ + B2+ (etapa rápida)
Com relação a este mecanismo, assinale a opção ERRADA.
