Questões Militares
Foram encontradas 266 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
DADOS:
Constante de Faraday= 96500 Coulombs/mol de elétrons
Massa molar do níquel=59 g/mol
Massa molar da prata=108 g/mol

Esse conjunto de cubas em série é ligado a uma bateria
durante um certo intervalo de tempo, sendo observado
um incremento de 54 g de massa de prata em um dos
eletrodos de prata. Desse modo, o incremento da massa
de níquel em um dos eletrodos de níquel é de
Dada a seguinte equação iônica de oxidorredução da reação, usualmente utilizada em etapas de sínteses químicas, envolvendo o íon dicromato (Cr2O72-) e o ácido oxálico (H2C2O4):
Cr2O72- + H2C2O4 + H+→ + Cr3+ + CO2 + H2O
Considerando a equação acima e o balanceamento de equações químicas por oxidorredução,
a soma total dos coeficientes mínimos e inteiros obtidos das espécies envolvidas e a substância
que atua como agente redutor são, respectivamente,
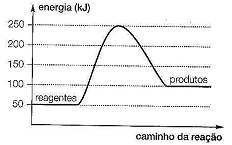
Considerando o gráfico anterior, referente ao diagrama energético de uma reação química, qual o valor da energia de ativação e o ΔH da reação respectivamente?
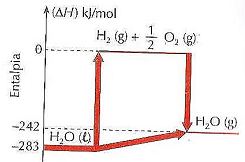
A partir do diagrama de entalpia, marque V para as afirmativas verdadeiras e F para as falsas.
( ) A quantidade de calor envolvido na decomposição de 126 g de H2O(l) → H2(g) + ½ O2(g) é 1.981 kJ/mol.
( ) H2O(l) → H2O(g) ΔH = –41 kJ/mol.
( ) H2(g) + ½ O2(g)→ H2O(g) ΔH = +242 kJ/mol.
A sequência está correta em
Fe2+(aq) + 2e– → Fe(s) E0 red = –0,44V.
Zn2+(aq) + 2e– → Zn(s) E0 red = –0,76V.
O2(g) + 4H+ (aq) + 4e– → 2H2O(l) E0 red = 1,23V.
Acerca do exposto anteriormente, analise as afirmativas a seguir.
I. A redução de O2 necessita de H+ , de forma que o aumento da concentração de H+ torna‐se a redução de O2 menos favorável.
II. O Fe2+ formado no anodo é eventualmente mais oxidado a Fe+3, que forma o óxido de ferro III hidratado.
III.O Fe2+ é mais facilmente reduzido que Zn2+.
Está(ão) correta(s) a(s) afirmativa(s)