Questões Militares
Foram encontradas 266 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
As semirreações de redução a seguir descrevem como pode ocorrer esse processo reacional:
Fe2+(aq) + 2e- → Fe(s) E0 = - 0,44 V
O2 (g) + 4H+ (aq) + 4e- → 2H2O (l) E0 = + 1,23 V
Em uma suposta pilha formada pelas duas semirreações, qual substância atuaria como agente redutor?
O quadro a seguir apresenta alguns combustíveis com suas respectivas entalpias molares de combustão:
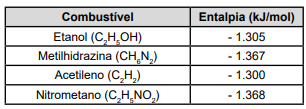
A partir desses dados, qual combustível pode liberar mais energia se, isoladamente, 100 g de cada substância for completamente queimada?
“Em 1836, o químico inglês John Frederic Daniell construiu uma pilha usando metais e soluções aquosas de sais. A pilha funcionava a partir de dois eletrodos interligados. O eletrodo é, geralmente, um sistema constituído por um metal imerso em uma solução aquosa de um sal formado pelos cátions desse metal.”
Adaptado de: FONSECA, Martha Reis Marques. Química. São Paulo: Editora FTD, 2007. v. 2: Físico-Química. p. 276.
Considere a representação da notação química da pilha de Daniell (usando eletrodos de cobre e zinco), de acordo com a União Internacional de Química Pura e Aplicada (IUPAC):
Zn (s) | Zn2+ (aq) (1 mol L-1) || Cu2+ (aq) (1 mol L-1) | Cu (s).
Dados os potenciais padrão de redução E0 Zn = - 0,76 V e E0 Cu = + 0,34 V, e considerando o funcionamento da referida pilha em condições padrão, afirma-se que
I – no eletrodo de cobre dessa pilha ocorre a corrosão da placa metálica de cobre.
II – a diferença de potencial (d.d.p.) teórica dessa pilha é de + 1,10 V.
III – nessa pilha os elétrons fluem no circuito externo, do eletrodo de zinco para o eletrodo de cobre.
IV – o símbolo de duas barras paralelas ( || ) representa a ponte salina (ou uma membrana porosa), cuja finalidade é manter as duas semicelas eletricamente neutras, por meio da migração de íons (corrente iônica).
V – a equação da reação global dessa pilha é Zn2+ (aq) + Cu (s) → Zn (s) + Cu2+ (aq).
Das afirmativas feitas, estão corretas apenas
Leia os textos a seguir e resolva a questão:
“Nas equações químicas, tanto as substâncias transformadas (reagentes) como as produzidas são representadas por fórmulas. As fórmulas das substâncias indicam elementos que as constituem e, também, a quantidade de átomos de cada elemento. O número que indica essa quantidade de átomos é chamado índice, que é anotado à direita do símbolo de cada elemento. (...)
A quantidade de cada substância que participa da reação é indicada por números escritos antes de suas fórmulas, denominados coeficientes estequiométricos, que devem ser os menores números inteiros possíveis.”
Fonte: USBERCO, João e SALVADOR, Edgard. Química. 14ª ed. Reform - São Paulo: Editora Saraiva, 2009. v. 1: Química Geral. p. 385.
“Em uma reação de oxidorredução, o mais comum é que uma espécie se oxide e outra se reduza. Porém, podem ocorrer casos com duas ou mais oxidações e apenas uma redução ou viceversa. De qualquer maneira, para o balanceamento desse tipo de reação, o princípio é sempre o mesmo: n° de elétrons perdidos = n° de elétrons recebidos.”
Fonte: USBERCO, João e SALVADOR, Edgard. Química. 14ª ed. Reform - São Paulo: Editora Saraiva, 2009. v. 2: Físico-Química. p. 250.
Considere a seguinte equação de reação química de oxidorredução não balanceada:
As2S3 + NH4OH + H2O2 → (NH4)3AsO4 + (NH4)2SO4 + H2O
Acerca desta reação química de oxidorredução e de suas espécies, são feitas as seguintes afirmativas:
I – O peróxido de hidrogênio é o agente redutor.
II – Após o devido balanceamento, o coeficiente estequiométrico da água é 20.
III – O arsênio da substância As2S3 é reduzido, enquanto o enxofre é oxidado.
IV – O (NH4)2SO4 é um sal cujo nome é sulfito de amônio.
V – Após o devido balanceamento, a soma de todos os coeficientes estequiométricos da equação é igual a 52.
Das afirmativas feitas, estão corretas apenas
Segundo as leis da radioatividade, um átomo de um elemento químico radioativo pode emitir várias partículas, como a alfa (α) e a beta (β), além de radiações de ondas eletromagnéticas, como a gama (ɣ). Considere as seguintes afirmativas acerca dessas emissões radioativas e de suas implicações:
I – A perda de uma partícula beta (β) por um átomo de um elemento radioativo ocasiona a formação de um átomo de número atômico maior.
II – A emissão de radiação gama (ɣ), a partir do núcleo de um átomo radioativo, não altera o número atômico e o número de massa deste átomo.
III – A emissão consecutiva de três partículas alfa (α) e duas beta (β), na desintegração do
isótopo radioativo 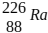 , gera o átomo do elemento químico
, gera o átomo do elemento químico 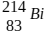 .
.
IV – O decaimento radioativo do átomo do elemento Roentgênio-272 (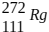 ), representado
pelo esquem
), representado
pelo esquem 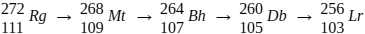 , denota a emissão exclusiva de
radiação gama (ɣ).
, denota a emissão exclusiva de
radiação gama (ɣ).
Das afirmativas feitas, estão corretas apenas