Questões Militares
Foram encontradas 519 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Observe a reação química a seguir.
CS2 (g) + 4H2 (g)  CH4 (g) + 2H2S
CH4 (g) + 2H2S
Em relação à reação química acima, assinale a opção que
apresenta a relação correta entre a lei da ação das massas,
as concentrações molares e a constante de equilíbrio da reação.
Observe a tabela abaixo.
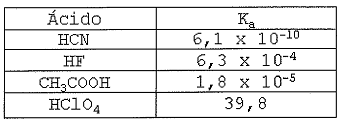
A tabela acima apresenta ácidos com suas respectivas constantes
de ionização (ka) . Assinale a opção que apresenta a
ordem decrescente de ionização desses ácidos.
Conversores catalíticos de automóveis são utilizados para reduzir a emissão de poluentes. Os gases resultantes da combustão no motor e o ar passam por substâncias catalisadoras que aceleram a transformação de monóxido de carbono (CO) em dióxido de carbono (CO2) e a decomposição de óxidos de nitrogênio (genericamente NxOy) em gás nitrogênio (N2) e gás oxigênio (O2). Em relação ao uso de catalisadores e as substâncias citadas no texto, são feitas as seguintes afirmações:
I – As reações de decomposição dos óxidos de nitrogênio a gás oxigênio e a gás nitrogênio ocorrem com variação no número de oxidação das espécies.
II – O CO2 é um óxido ácido que quando reage com a água forma o ácido carbônico.
III – Catalisadores são substâncias que iniciam as reações químicas que seriam impossíveis sem eles, aumentando a velocidade e também a energia de ativação da reação.
IV – O monóxido de carbono é um óxido básico que ao reagir com a água forma uma base.
V – A molécula do gás carbônico apresenta geometria espacial angular.
Das afirmativas feitas estão corretas apenas:
Os corais fixam-se sobre uma base de carbonato de cálcio (CaCO3), produzido por eles mesmos. O carbonato de cálcio em contato com a água do mar e com o gás carbônico dissolvido pode estabelecer o seguinte equilíbrio químico para a formação do hidrogenocarbonato de cálcio:
CaCO3 (s) + CO2 (g) + H2O (l) 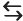 Ca(HCO3)2 (aq)
Ca(HCO3)2 (aq)
Considerando um sistema fechado onde ocorre o equilíbrio químico da reação mostrada acima,
assinale a alternativa correta.
Uma das aplicações da trinitroglicerina, cuja fórmula é C3H3N3O9, é a confecção de explosivos. Sua decomposição enérgica gera como produtos os gases nitrogênio, dióxido de carbono e oxigênio, além de água, conforme mostra a equação da reação a seguir:
4 C3H3N3O9 (l) → 6 N2 (g) + 12 CO2 (g) + 1 O2 (g) + 10 H2O (l).
Além de explosivo, a trinitroglicerina também é utilizada como princípio ativo de medicamentos no tratamento de angina, uma doença que acomete o coração. Medicamentos usados no tratamento da angina usam uma dose padrão de 0,6 mg de trinitroglicerina na formulação. Considerando os dados termoquímicos da reação a 25 ºC e 1 atm e supondo que essa massa de trinitroglicerina sofra uma reação de decomposição completa, a energia liberada seria aproximadamente de
Dados: massas atômicas: C = 12 u; H = 1 u; N = 14 u; O = 16 u.
∆Hof (H2O) = - 286 kJ/mol; ∆Hof
(CO2) = - 394 kJ/mol; ∆Hof
(C3H5N3O9) = - 353,6 kJ/mol