Questões Militares
Foram encontradas 456 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Uma quantidade de 5828 g de mistura de óxido de sódio(Na2O) e óxido de potássio(K2O) foi tratada com uma solução de ácido clorídrico que continha 300 mols de HCl. Admitindo-se que toda a mistura de óxidos reagiu com parte do HCl, e que o excesso de HCl necessitou de 144 mols de hidróxido de sódio(NaOH) para ser totalmente neutralizado, então a composição percentual, em massa de Na2O e de K2O era, respectivamente,

São dadas as seguintes informações relativas às reações que ocorrem à temperatura de 25 °C e à pressão de 1 atm.

As equações químicas a seguir representam o processo de síntese dos óxidos de bário e alumínio e suas respectivas entalpias de transformação.
2Ba(s) + O2 (g) → 2 BaO(s) ΔHº = –1.107 kJ
2Al(s) + 3/2O2 (g) → Al2 O3 (s) ΔHº = –1.676 kJ
O metal bário é produzido pela reação do metal alumínio com óxido de bário.
A partir dessas informações, a variação da entalpia para a reação de produção do metal bário é igual a:
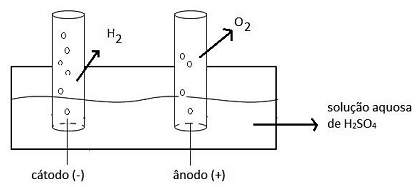
Com relação ao experimento, dentre as substâncias iniciais e as que foram formadas no processo de eletrólise da água, são consideradas substância simples, composta e mistura, respectivamente:
Em 2012, uma carreta carregada com ácido sulfúrico (H2 SO4 ) tombou na Br-381. Sabe-se que o ácido sulfúrico tem as seguintes propriedades:

Considerando que nesse acidente o derramamento de ácido foi de 20 mil litros, qual a massa, em gramas,
aproximada de bicarbonato de sódio (NaHCO3
) necessária para neutralizar totalmente o ácido?