Questões Militares
Foram encontradas 321 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
A tabela abaixo indica valores das velocidades da reação (v) em três experimentos e as correspondentes concentrações em mol/L dos reagentes X e Y em idênticas condições.

O processo químico é representado pela equação abaixo, na qual a, b e c representam seus coeficientes.
a X + b y → c Z
A equação da velocidade desse processo é:
H2O(l) → H2O(v) ΔH= + 44kj/mol
A quantidade de calor necessária para provocar a vaporização de 900 mL de água líquida nesse processo é:
Dados:
Densidade da água = 1,0 g/ml
Massas atômicas: H=1 u; 0 = 16 u
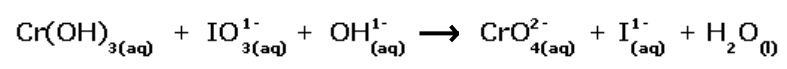
Considerando o método de balanceamento de equações químicas por oxi-redução, a soma total dos coeficientes mínimos e inteiros das espécies envolvidas, após o balanceamento da equação iônica, e o agente oxidante são, respectivamente,

Admita a variação de concentração em mol por litro (mol·L-1) do monóxido de nitrogênio (NO) em função do tempo em segundos (s), conforme os dados, da tabela abaixo:
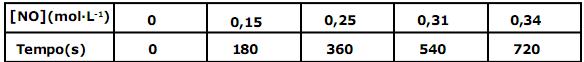
A velocidade média, em função do monóxido de nitrogênio (NO), e a velocidade média da reação acima representada, no intervalo de tempo de 6 a 9 minutos (min), são, respectivamente, em mol·L-1·min-1:
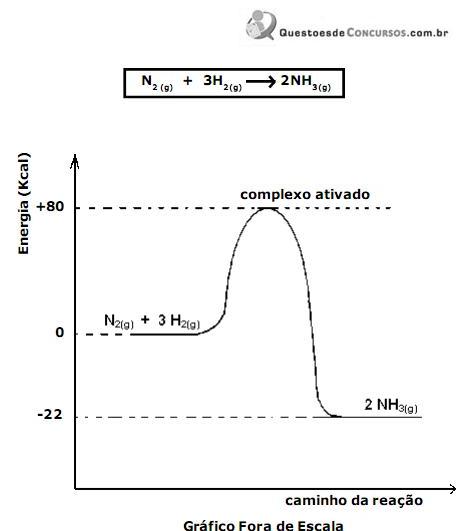
Relativo ao gráfico envolvendo essa reação e suas informações, são feitas as seguintes afirmações:
I - O valor da energia envolvida por um mol de NH3 formado é 22 kcal.
II - O valor da energia de ativação dessa reação é 80 kcal.
III - O processo que envolve a reação N2(g) + 3H2(g) → 2NH3(g) é endotérmico.
Das afirmações feitas, está(ão) correta(s)