Questões Militares Comentadas por alunos sobre grandezas: massa, volume, mol, massa molar, constante de avogadro e estequiometria. em química
Foram encontradas 165 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
O gráfico a seguir apresenta os resultados obtidos para a relação entre massa e volume de cada uma dessas amostras, medidos a 25ºC.
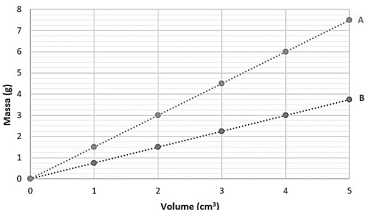
A partir dos dados apresentados é possível afirmar que, nessa temperatura, a razão entre as densidades das amostras A e B é igual a
Na + CH3 CH2 OH → CH3 CH2 ONa + H2
Considerando que nas CATP (Condições Ambientais de Temperatura e Pressão) 1 mol de qualquer gás ocupa 25 L, o volume de H2 produzido, quando reagem 1 g de sódio e 1 g etanol, e a massa do excesso de reagente são, respectivamente,
Pb(NO3)2 + 2KI → PbI2 + 2KNO3 CH3NH2 + HI → CH3NH3I PbI2 + CH3NH3I → CH3NH3PbI3
Os seguintes reagentes foram empregados na síntese: 0,6 mol de Pb(NO3)2; 0,8 mol de KI; 0,7 mol de CH3NH2; e 0,8 mol de HI. Nessas condições, qual será a quantidade máxima da perovskita CH3NH3PbI3 produzida?
Considerando o nível de glicose citado de 50mg/dL (considere 1dL = 0,1L), é CORRETO afirmar que a conversão desta unidade de concentração em mmol/L de glicose chegará ao valor aproximado de: