Questões Militares Comentadas por alunos sobre termodinâmica e equilíbrio de fases em engenharia química e química industrial
Foram encontradas 35 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Analise a equação a seguir.
ΔU = q + w
A primeira Lei da Termodinâmica estabelece que a energia
interna de um sistema pode ser expressa pela equação acima.
Com base nos princípios da Termodinâmica e nessa equação,
assinale a opção correta.
Um mol de gás hidrogênio, a 27 °C em um sistema fechado, se expande isotermicamente contra uma pressão externa constante igual a 1 atm, até duplicar o seu volume inicial. Qual é o calor necessário para manter constante a temperatura do gás, sabendo que a pressão final do gás é 1 atm?
Dados : ΔU = Q - W
W = PextΔV
PV = nRT
T(K) = T(°C) + 273
R = 0,082 atm•L • mol-1 • K-1
1atm = 105 N • m-2
A figura apresentada a seguir representa um diagrama de equilíbrio de fases (hipotético) das ligas A-B.
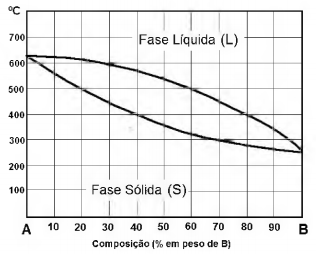
Uma determinada peça composta da liga A-B foi aquecida em condições de equilíbrio até a temperatura de 500°C e
fundiu parcialmente. Sabendo que nesta temperatura a fase sólida possui 80kg do elemento químico B e a fase
líquida possui 40kg do elemento químico A, qual é a percentagem em peso de B da liga que compõe essa peça?
Considere as supostas variações de entropia (∆S) nos processos abaixo:
I) cristalização do sal comum (∆S > 0)
II) sublimação da naftalina (naftaleno ) ( ∆S > 0)
III) mistura de água e álcool ( ∆S < 0)
IV) ferro (s) ferro (l) ( ∆S > 0)
ferro (l) ( ∆S > 0)
V) ar 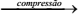 ar comprimido (∆S < 0)
ar comprimido (∆S < 0)
As variações de entropia indicadas nos processos que estão corretas são: