Questões Militares
Foram encontradas 1.485 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Quando um átomo, ou um grupo de átomos, perde a neutralidade elétrica, passa a ser denominado de íon. Sendo assim, o íon é formado quando o átomo (ou grupo de átomos) ganha ou perde elétrons. Logicamente, esse fato interfere na distribuição eletrônica da espécie química. Todavia, várias espécies químicas podem possuir a mesma distribuição eletrônica.
Considere as espécies químicas listadas na tabela a seguir:

A distribuição eletrônica 1s2, 2s2, 2p6, 3s2, 3p6 (segundo o Diagrama de Linus Pauling) pode
corresponder, apenas, à distribuição eletrônica das espécies
"Sempre que uma substância muda de fase de agregação, a temperatura permanece constante enquanto a mudança se processa, desde que a pressão permaneça constante".
FONSECA Martha Reis Marques da, Química Geral, São Paulo: Ed FTD, 2007, pág 41.
O gráfico abaixo representa a mudança de fase de agregação de uma substância pura com o passar do tempo, em função da variação de temperatura, observada ao se aquecer uma substância X durante algum tempo, sob pressão constante.
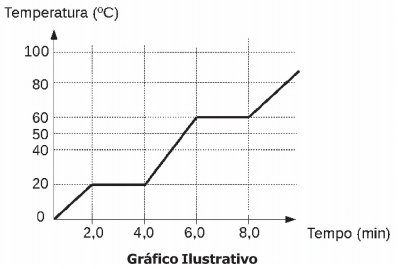
Tomando-se como base o gráfico, analise as seguintes afirmativas:
I - entre 0 °C e 19 °C, a substância X encontra-se na fase sólida;
II - o intervalo de 2,0 min a 4,0 min corresponde à condensação da substância X;
III - a temperatura de 60 °C corresponde à temperatura de ebulição da substância X;
IV - no intervalo de 40 °C a 50 °C, a substância X encontra-se na fase líquida.
Estão corretas apenas as afirmativas
Conversores catalíticos (catalisadores) de automóveis são utilizados para reduzir a emissão de poluentes tóxicos. Poluentes de elevada toxicidade são convertidos a compostos menos tóxicos. Nesses conversores, os gases resultantes da combustão no motor e o ar passam por substâncias catalisadoras. Essas substâncias aceleram, por exemplo, a conversão de monóxido de carbono (CO) em dióxido de carbono (CO2) e a decomposição de óxidos de nitrogênio como o NO, N2O e o NO2 (denominados NOx) em gás nitrogênio (N2) e gás oxigênio (O2). Referente às substâncias citadas no texto e às características de catalisadores, são feitas as seguintes afirmativas:
I - a decomposição catalítica de óxidos de nitrogênio produzindo o gás oxigênio e o gás nitrogênio é classificada como uma reação de oxidorredução;
II - o CO2 é um óxido ácido que, ao reagir com água, forma o ácido carbônico;
III - catalisadores são substâncias que iniciam as reações químicas que seriam impossíveis sem eles, aumentando a velocidade e também a energia de ativação da reação;
IV - o CO é um óxido básico que, ao reagir com água, forma uma base;
V - a molécula do gás carbônico (CO2) apresenta geometria espacial angular.
Das afirmativas feitas estão corretas apenas a
A gasolina é um combustível constituído por uma mistura de diversos compostos químicos, principalmente hidrocarbonetos. Estes compostos apresentam volatilidade elevada e geram facilmente vapores inflamáveis.
Em um motor automotivo, a mistura de ar e vapores inflamáveis de gasolina é comprimida por um pistão dentro de um cilindro e posteriormente sofre ignição por uma centelha elétrica (faísca) produzida pela vela do motor.
Adaptado de: BROWN, Theodore; L. LEMAY, H Eugene; BURSTEN, Bruce E. Química a Ciência Central, 9ª edição, Editora Prentice-Hall, 2005, pág 926.
Pode-se afirmar que a centelha elétrica produzida pela vela do veículo neste evento tem a
função química de
A emissão de gases derivados do enxofre, como o dióxido de enxofre (SO2), pode ocasionar uma série de problemas ambientais e a destruição de materiais como rochas e monumentos à base de calcita (carbonato de cálcio). Essa destruição ocasiona reações com a emissão de outros gases, como o gás carbônico (CO2), potencializando o efeito poluente. Considerando as equações das reações sucessivas a 27 °C e 1 atm, admitindo-se os gases como ideais e as reações completas, o volume de CO2 produzido a partir da utilização de 2 toneladas de SO2 como reagente é, aproximadamente,
Dados
Massas Atômicas: S = 32 u ; O = 16 u ; H = 1 u ; C = 12 u ; Ca = 40 u
Constante dos gases ideais: R = 0,082 atm L
L mol-1
mol-1 K-1
K-1
Volume molar nas condições em que ocorreu a reação (27° e 1 atm) = 24,6 L/mol
SO2 (g) + 1/2 O2 (g) → SO3 (g) (equação I)
SO3 (g) + H2O (ℓ) → H2SO4 (ℓ) (equação II)
H2SO4 (ℓ) + CaCO3 (s) → CaSO4 (s) + H2O (ℓ) + CO2 (g) (equação III)