Questões Militares
Foram encontradas 1.485 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Dada a seguinte equação iônica de oxidorredução:
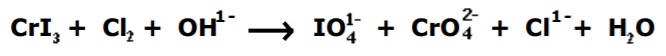
Considerando o balanceamento de equações químicas por oxidorredução, a soma total dos coeficientes mínimos e inteiros obtidos das espécies envolvidas e o(s) elemento(s) que sofrem oxidação, são, respectivamente,
(25 °C e 1 atm), expressas em kJ · mol -1.

A alternativa que corresponde ao valor da entalpia da reação abaixo, nas condições-padrão, é:
4 C(grafita)(s) + 5 H2(g) → C4H10(g)
Bicarbonato 100,0
Cálcio 22,0
Sódio 8,98
Nitrato 4,11
Sulfato 6,00
Magnésio 3,26
Potássio 2,70
Cloreto 0,73
Fluoreto 0,34
Sabe-se que a massa molar do íon sulfato (SO42-) é de 96 g/mol. A quantidade de mols de íons sulfato contida em 16 L dessa água mineral é:
Cl2(g) + OH1-(aq) → Cl1-(aq) + ClO31-(aq) + H2O(l)
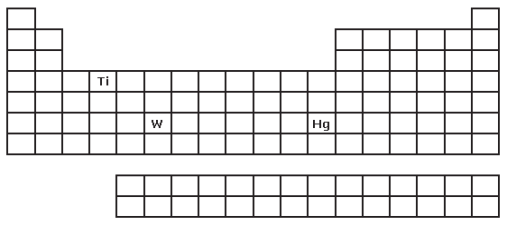
I) É freqüentemente usado em lâmpadas incandescentes, tem elevado ponto de fusão e número atômico igual 74.
II) É líquido nas condições ambiente (25º C e 1 atm) e utilizado em barômetros, em lâmpadas especiais e em odontologia.
III) Possui número atômico 22 e está na família 4 da Tabela Periódica. Algumas de suas utilizações podem ser assim exemplificadas: aplicação de próteses em joelhos e quadris; colocação de pinos para fixação entre a mandíbula e a prótese dentária.
Os metais descritos em I, II e III são, respectivamente: