Questões Militares
Comentadas para cadete do exército
Foram encontradas 836 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
O ácido etanoico, também denominado usualmente de ácido acético, é um ácido orgânico e uma das substâncias componentes do vinagre. Considerando-se a substância ácido etanoico, pode-se afirmar que:
I – É um composto cuja fórmula molecular é C2H6O.
II – Possui apenas ligações covalentes polares entre seus átomos.
III – Possui um carbono com hibridização sp2.
IV – Possui dois carbonos assimétricos (quiral).
V – O anidrido etanoico (acético) é isômero de cadeia do ácido etanoico (acético).
VI – Pode ser obtido pela oxidação enérgica do but-2-eno em presença do permanganato de potássio e ácido concentrado.
VII – Em condições adequadas, sua reação com sódio metálico produz etanoato de sódio e libera H2.
Das afirmativas feitas, estão corretas apenas
Modelo Característica(s) do Modelo I Átomo contém espaços vazios. No centro do átomo existe um núcleo muito pequeno e denso. O núcleo do átomo tem carga positiva. Para equilíbrio de cargas, existem elétrons ao redor do núcleo. II Átomos maciços e indivisíveis. III Elétrons movimentam-se em órbitas circulares em torno do núcleo atômico central. A energia do elétron é a soma de sua energia cinética (movimento) e potencial (posição). Essa energia não pode ter um valor qualquer, mas apenas valores que sejam múltiplos de um quantum (ou de um fóton). Os elétrons percorrem apenas órbitas permitidas.
A alternativa que apresenta a correta correlação entre o cientista proponente e o modelo atômico por ele proposto é
Gases apresentam um fenômeno chamado de difusão de gases.
“Difusão gasosa é o movimento espontâneo das partículas de um gás de se espalharem uniformemente em meio das partículas de um outro gás ou de atravessarem uma parede porosa.
Quando gases diferentes (A e B) estão a uma mesma temperatura, para uma quantidade de matéria igual a 1 mol de gás A e 1 mol de gás B, tem-se que a massa do gás A (ma) será igual à massa molar do gás A (Ma), e a massa do gás B (mb) será igual à massa molar do gás B (Mb).”
FONSECA, Martha Reis Marques da, Química Geral, São Paulo, Ed FTD, 2007,
Pág. 110
Considere que, em determinadas condições de temperatura e pressão, a velocidade de difusão de 1 mol do gás hidrogênio (H2) seja de 28 km/min. Nestas mesmas condições a velocidade (em km/h) de 1 mol do gás metano (CH4) é de
Dado: √2 = 1,4
“No fenômeno físico, a composição da matéria é preservada, ou seja, permanece a mesma antes e depois da ocorrência do fenômeno”.
“Reação química é toda transformação que modifica a natureza da matéria (fenômenos químicos)”.
“No fenômeno químico, a composição da matéria é alterada: sua composição antes de ocorrer o fenômeno é diferente da que resulta no final”.
FONSECA, Martha Reis Marques da, Química Geral, São Paulo, Ed FTD, 2007, Pág. 24 e 61.
Considere os conceitos supracitados e as transformações representadas pelas equações químicas a seguir:
I – CaCO3 (s) → CaO (s) + CO2 (g)
II – H2O (l) →H2O (g)
III – H2 (g) + O2 (g) → H2O (g)
IV – C(grafite) + O2 (g) → CO2 (g)
Correspondem a reações químicas apenas as transformações
“Solução saturada: solução que contém a quantidade máxima de soluto em determinada quantidade de solvente, a determinada temperatura; a relação entre quantidades máximas de soluto e quantidade de solvente é denominada de coeficiente de solubilidade”.
“Solução insaturada: quando a solução contém uma quantidade de soluto inferior ao seu coeficiente de solubilidade, na temperatura em que se encontra a solução”.
“Solução supersaturada: quando a solução contém uma quantidade de soluto dissolvido superior ao seu coeficiente de solubilidade, na temperatura em que se ela se encontra. É instável” .
USBERCO, João e SALVADOR, Edgard, Físico-química, São Paulo, Ed Saraiva, 2009, Pág. 18
FONSECA, Martha Reis Marques da, Química Geral, São Paulo, Ed FTD, 2007, Pág. 18 e 19.
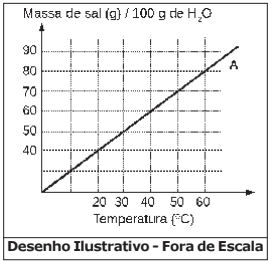
Considere o gráfico da curva de solubilidade em função da temperatura para um sal hipotético A. No gráfico, a linha contínua representa a solubilidade máxima do soluto (sal A) em 100 g de água na temperatura correspondente.
Acerca desse gráfico e processo de solubilidade são feitas as seguintes afirmativas:
I – Na temperatura de 20 ºC, misturando-se 50 g do sal A em 100 g de água, ter-se-á um sistema heterogêneo.
II – Na temperatura de 40 ºC, a adição de 50 g do sal A em 100 g de água produzirá uma solução insaturada.
III – 200 g de água dissolvem totalmente 90 g do sal A a 30 ºC.
IV – Uma solução contendo 60 g do sal A em 100 g de água será saturada em 60 ºC.
Das afirmativas feitas estão corretas apenas