Questões Militares
Para ita
Foram encontradas 1.149 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Uma lâmpada incandescente comum consiste de um bulbo de vidro preenchido com um gás e de um filamento metálico que se aquece e emite luz quando percorrido por corrente elétrica.
Assinale a opção com a afirmação ERRADA a respeito de características que o filamento metálico deve apresentar para o funcionamento adequado da lâmpada.
Sabe-se que a 25 °C as entalpias de combustão (em kJ mol−1) de grafita, gás hidrogênio e gás metano são, respectivamente: –393,5; –285,9 e –890,5. Assinale a alternativa que apresenta o valor CORRETO da entalpia da seguinte reação:
C(grafita) + 2H2 (g) → CH4(g)
Uma solução aquosa saturada em fosfato de estrôncio [Sr3(PO4)2] está em equilíbrio químico à temperatura de 25 °C, e a concentração de equilíbrio do íon estrôncio, nesse sistema, é de 7,5 x 10–7 mol L–1.
Considerando-se que ambos os reagentes (água e sal inorgânico) são quimicamente puros, assinale a alternativa CORRETA com o valor do pKPS(25ºC) do Sr3(PO4)2.
Dado: KPS = constante do produto de solubilidade.
Em cinco béqueres foram adicionados 50 mL de uma solução de referência, que consiste de uma solução aquosa saturada em cloreto de prata, contendo corpo de fundo, a 25 °C e 1 atm. A cada béquer, foram adicionados 50 mL de uma solução aquosa diluída diferente, dentre as seguintes:
I. Solução de cloreto de sódio a 25 °C.
II. Solução de Glicose a 25 °C.
III. Solução de Iodeto de sódio a 25 °C.
IV. Solução de Nitrato de prata a 25 °C.
V. Solução de Sacarose a 50 °C.
Considere que o corpo de fundo permanece em contato com as soluções após rápida homogeneização das
misturas aquosas e que não ocorre formação de óxido de prata sólido. Nestas condições, assinale a opção que
indica a(s) solução(ões), dentre as acima relacionadas, que altera(m) a constante de equilíbrio da solução de
referência.
Considere o seguinte mecanismo de reação genérica:
A4++ B2+ → A3+ + B3+ (etapa lenta)
A4+ + B3+ → A3+ + B4+ (etapa rápida)
C+ + B4+ → C3+ + B2+ (etapa rápida)
Com relação a este mecanismo, assinale a opção ERRADA.
Considere os seguintes líquidos, todos a 25 °C:
I. Cu(NO3)2 (aq)
II. CS2(l )
III. CH3CO2H(aq)
IV. CH3(CH2)16 CH2OH(l )
V. HCl (aq)
VI. C6H6( l )
Assinale a opção que indica o(s) líquido(s) solúvel(eis) em tetracloreto de carbono.
A seguinte reação não-balanceada e incompleta ocorre em meio ácido:
(Cr2O7 )-2 + (C2 O4)-2 → Cr3+ + CO2
A soma dos coeficientes estequiométricos da reação completa e balanceada é igual a
Uma barra de ferro e um fio de platina, conectados eletricamente a um voltímetro de alta
impedância, são parcialmente imersos em uma mistura de soluções aquosas de FeSO4 (1,0 mol L–1) e HCl isenta de oxigênio. Um fluxo de gás hidrogênio é mantido constante sobre a parte imersa da superfície da
platina, com pressão nominal (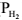 ) de 1,0 atm, e a força eletromotriz medida a 25 °C é igual a 0,292 V.
) de 1,0 atm, e a força eletromotriz medida a 25 °C é igual a 0,292 V.
Considerando-se que ambos os metais são quimicamente puros e que a platina é o polo positivo do elemento galvânico formado, assinale a opção CORRETA que apresenta o valor calculado do pH desse meio aquoso.
Dados: 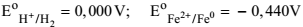
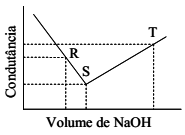
Uma solução aquosa de HCl 0,1 mol L–1 foi titulada com uma solução aquosa de NaOH 0,1 mol L–1. A figura ao lado apresenta a curva de titulação obtida em relação à condutância da solução de HCl em função do volume de NaOH adicionado.
Com base nas informações apresentadas nesta figura, assinale a opção ERRADA.
Historicamente, a teoria atômica recebeu várias contribuições de cientistas.
Assinale a opção que apresenta, na ordem cronológica CORRETA, os nomes de cientistas que são apontados como autores de modelos atômicos.
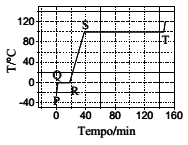
A figura ao lado apresenta a curva de aquecimento de 100 g de uma substância pura genérica no estado sólido. Sabe-se que calor é fornecido a uma velocidade constante de 500 cal min–1. Admite-se que não há perda de calor para o meio ambiente, que a pressão é de 1 atm durante toda a transformação e que a substância sólida apresenta apenas uma fase cristalina. Considere que sejam feitas as seguintes afirmações em relação aos estágios de aquecimento descritos na figura:
I. No segmento PQ ocorre aumento da energia cinética das moléculas.
II. No segmento QR ocorre aumento da energia potencial.
III. O segmento QR é menor que o segmento ST porque o calor de fusão da substância é menor que o seu calor de vaporização.
IV. O segmento RS tem inclinação menor que o segmento PQ porque o calor específico do sólido é maior que o calor específico do líquido.
Das afirmações acima, está(ão) ERRADA(S):
No último livro que publicou em vida, Teia (1996), a escritora Orides Fontela escreveu o poema ao lado.

Podemos afirmar que:
I. nem a parte I nem a II indicam que o pássaro “joão-de-barro” pode ser visto como metáfora de um determinado tipo social.
II. apenas a parte III sugere que o trabalho feito pelo joão-de-barro aproxima-se daquele feito por um operário.
III. o poema, em seu todo, aproxima metaforicamente o “joão-de-barro” de um trabalhador brasileiro (um “João”, como o título indica).
IV. como no caso do pássaro, também para o operário vale a idéia de que o homem faz o trabalho e o trabalho faz o homem.
Estão corretas apenas as afirmações:
O poema ao lado faz parte da obra Livro sobre nada (1996), de Manoel de Barros:
A ciência pode classificar e nomear os órgãos de um sabiá
mas não pode medir seus encantos.
A ciência não pode calcular quantos cavalos de força
existem
nos encantos de um sabiá.
Quem acumula muita informação perde o condão de
adivinhar: divinare.
Os sabiás divinam.
É certo dizer que estamos diante de um poema
