Questões Militares
Para aluno do ita
Foram encontradas 869 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Os argumentos principais das soluções da equação em z;
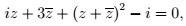
pertencem a
Se z é uma solução da equação em C,
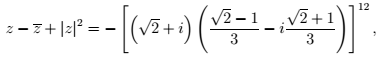
pode-se afirmar que
Considere conjuntos A, B ⊂ R e C ⊂ (A ∪B). Se A ∪B , A ∩ C e B ∩ C são os domínios
das funções reais definidas por 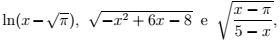 respectivamente, pode-se
afirmar que
respectivamente, pode-se
afirmar que
Considere as afirmações abaixo relativas a conjuntos A, B e C quaisquer:
I. A negação de x ∈ A ∩B é: x ∉ A ou x ∉ B.
II. A ∩ (B ∪ C) = (A ∩ B) ∪ (A ∩ C).
III. (A\ B) ∪ (B\ A) = (A ∪ B)\ (A ∩ B).
Destas, é (são) falsa(s)
Considere o composto aromático do tipo C6H5Y, em que Y representa um grupo funcional ligado ao anel.
Assinale a opção ERRADA com relação ao(s) produto(s) preferencialmente formado(s) durante a reação de nitração deste tipo de composto nas condições experimentais apropriadas.
Considere duas reações químicas, mantidas à temperatura e pressão ambientes, descritas pelas equações abaixo:
I. H2(g) + 1/2 O2(g) → H2O(g)
ΙΙ. H2(g) + 1/2O2(g) → H2O(l )
Assinale a opção que apresenta a afirmação ERRADA sobre estas reações.
Em um processo de eletrodeposição de níquel, empregou-se um eletrodo ativo de níquel e um eletrodo de cobre, ambos parcialmente imersos em uma solução aquosa contendo sais de níquel (cloreto e sulfato) dissolvidos, sendo este eletrólito tamponado com ácido bórico. No decorrer do processo, conduzido à temperatura de 55 °C e pressão de 1 atm, níquel metálico depositou-se sobre a superfície do eletrodo de cobre. Considere que as seguintes afirmações sejam feitas:
I. Ocorre formação de gás cloro no eletrodo de cobre.
II. A concentração de íons cobre aumenta na solução eletrolítica.
III. Ocorre formação de hidrogênio gasoso no eletrodo de níquel.
IV. O ácido bórico promove a precipitação de níquel na forma de produto insolúvel no meio aquoso.
Com relação ao processo de eletrodeposição acima descrito, assinale a opção CORRETA.
Uma lâmpada incandescente comum consiste de um bulbo de vidro preenchido com um gás e de um filamento metálico que se aquece e emite luz quando percorrido por corrente elétrica.
Assinale a opção com a afirmação ERRADA a respeito de características que o filamento metálico deve apresentar para o funcionamento adequado da lâmpada.
Sabe-se que a 25 °C as entalpias de combustão (em kJ mol−1) de grafita, gás hidrogênio e gás metano são, respectivamente: –393,5; –285,9 e –890,5. Assinale a alternativa que apresenta o valor CORRETO da entalpia da seguinte reação:
C(grafita) + 2H2 (g) → CH4(g)
Uma solução aquosa saturada em fosfato de estrôncio [Sr3(PO4)2] está em equilíbrio químico à temperatura de 25 °C, e a concentração de equilíbrio do íon estrôncio, nesse sistema, é de 7,5 x 10–7 mol L–1.
Considerando-se que ambos os reagentes (água e sal inorgânico) são quimicamente puros, assinale a alternativa CORRETA com o valor do pKPS(25ºC) do Sr3(PO4)2.
Dado: KPS = constante do produto de solubilidade.
Em cinco béqueres foram adicionados 50 mL de uma solução de referência, que consiste de uma solução aquosa saturada em cloreto de prata, contendo corpo de fundo, a 25 °C e 1 atm. A cada béquer, foram adicionados 50 mL de uma solução aquosa diluída diferente, dentre as seguintes:
I. Solução de cloreto de sódio a 25 °C.
II. Solução de Glicose a 25 °C.
III. Solução de Iodeto de sódio a 25 °C.
IV. Solução de Nitrato de prata a 25 °C.
V. Solução de Sacarose a 50 °C.
Considere que o corpo de fundo permanece em contato com as soluções após rápida homogeneização das
misturas aquosas e que não ocorre formação de óxido de prata sólido. Nestas condições, assinale a opção que
indica a(s) solução(ões), dentre as acima relacionadas, que altera(m) a constante de equilíbrio da solução de
referência.
Considere o seguinte mecanismo de reação genérica:
A4++ B2+ → A3+ + B3+ (etapa lenta)
A4+ + B3+ → A3+ + B4+ (etapa rápida)
C+ + B4+ → C3+ + B2+ (etapa rápida)
Com relação a este mecanismo, assinale a opção ERRADA.
Considere os seguintes líquidos, todos a 25 °C:
I. Cu(NO3)2 (aq)
II. CS2(l )
III. CH3CO2H(aq)
IV. CH3(CH2)16 CH2OH(l )
V. HCl (aq)
VI. C6H6( l )
Assinale a opção que indica o(s) líquido(s) solúvel(eis) em tetracloreto de carbono.
A seguinte reação não-balanceada e incompleta ocorre em meio ácido:
(Cr2O7 )-2 + (C2 O4)-2 → Cr3+ + CO2
A soma dos coeficientes estequiométricos da reação completa e balanceada é igual a
Uma barra de ferro e um fio de platina, conectados eletricamente a um voltímetro de alta
impedância, são parcialmente imersos em uma mistura de soluções aquosas de FeSO4 (1,0 mol L–1) e HCl isenta de oxigênio. Um fluxo de gás hidrogênio é mantido constante sobre a parte imersa da superfície da
platina, com pressão nominal (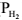 ) de 1,0 atm, e a força eletromotriz medida a 25 °C é igual a 0,292 V.
) de 1,0 atm, e a força eletromotriz medida a 25 °C é igual a 0,292 V.
Considerando-se que ambos os metais são quimicamente puros e que a platina é o polo positivo do elemento galvânico formado, assinale a opção CORRETA que apresenta o valor calculado do pH desse meio aquoso.
Dados: