Questões Militares
Para engenharia química
Foram encontradas 255 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
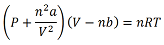
Na equação, as variáveis P, V, n, R, T são usuais, mas os parâmetros (a) e (b) são conhecidos como constantes de Van Der Waals.
Considerar R: 0,0821 atm · L · K−1 · mol−1
Tabela – Constantes de Van Der Waals
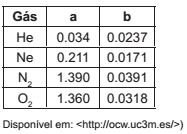
Utilizando a equação de Van Der Waals para gases reais, calcule a pressão real exercida por 16 gramas de gás oxigênio que se encontra em um recipiente de 1L a 27°C.
Para misturas binárias, as condições de equilíbrio para várias composições podem ser facilmente visualizadas em diagramas do tipo Txy e xy, à pressão constante, ou Pxy e xy, à temperatura constante.
Diagrama binário para a mistura Benzeno e Tolueno.
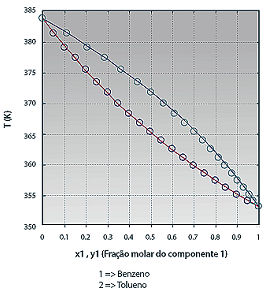
(Disponível em: <http://labvirtual.eq.uc.pt> )
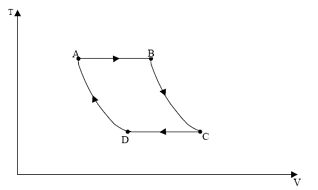
Com base nesse gráfico, é correto afirmar que entre os pontos
Informe se é verdadeiro (V) ou falso (F) o que se afirma abaixo sobre as propriedades termodinâmicas.
( ) Ponto de orvalho é a temperatura na qual se inicia a condensação da mistura.
( ) Ponto de bolha é a temperatura na qual se inicia a ebulição do líquido puro.
( ) Quando a mistura está no ponto de bolha, dizemos que é um líquido insaturado.
( ) Se a mistura estiver aquecida acima do ponto de bolha, dizemos que é vapor superaquecido
A alternativa que apresenta a sequência correta é
Uma amostra de gás ideal sofreu uma transformação termodinâmica à pressão constante igual a 30 N/m2 . O volume e a temperatura absoluta variam como indica o gráfico a seguir.
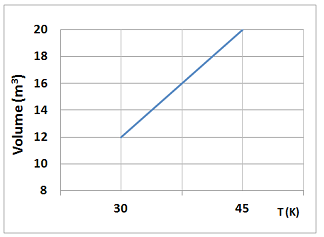
Sabendo-se que, nessa transformação, o gás absorve 400J de calor, pode-se afirmar que a variação de sua
energia interna é de
O gráfico a seguir representa a variação de concentração das espécies A, B e C com o tempo:
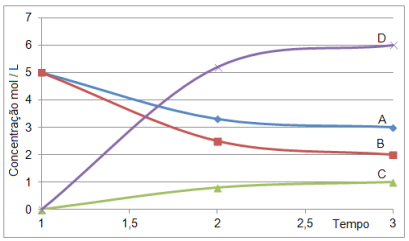
Mediante a reação representada pelo gráfico, marque a alternativa que representa corretamente a equação
química.
Um catalisador é uma substância que faz variar a velocidade de uma reação química sem que ele próprio sofra uma variação química permanente no processo. Os catalisadores são bem comuns, muitas reações na indústria química ocorrem com a ajuda de catalisadores.
Informe se é verdadeiro (V) ou falso (F) o que se afirma abaixo sobre a Catálise Homogênea.
( ) Os catalisadores podem agir aumentando a velocidade de reação, mas não alteram o número de colisões efetivas.
( ) Os átomos de cloro são catalisadores para a destruição do ozônio.
( ) Na ausência do catalisador, as reações ocorrem de maneira extremamente lenta.
A alternativa que apresenta a sequência correta é
Os confinamentos nos quais ocorrem reações químicas são chamados reatores. Existem vários tipos de reatores químicos e várias maneiras de classificá-los.
Informe se é verdadeiro (V) ou falso (F) o que se afirma abaixo sobre Reatores.
( ) O reator em batelada é um tipo de vaso largamente usado em processos industriais. As vantagens de um reator de batelada residem em sua versatilidade.
( ) Reator perfeitamente agitado (RPA) é um tipo de reator ideal comum em engenharia química. Frequentemente refere-se a um modelo usado para estimar as variáveis principais de uma operação unitária.
( ) Reator de fluxo em pistão (PFR) é usado para descrever reações químicas em sistemas de fluxo contínuo.
( ) A manutenção de reatores RPA é mais cara do que a manutenção dos reatores RFP.
( ) Reatores de fluxo em pistão têm uma conversão por unidade de volume baixa, mas operam por longos períodos de tempo sem manutenção.
A alternativa que apresenta a sequência correta é
Em qualquer sistema de bombeamento, o papel da bomba é proporcionar pressão suficiente para superar a pressão de funcionamento do sistema a fim de mover o fluido a uma taxa de fluxo necessária. A pressão de funcionamento do sistema é uma função do fluxo através do sistema e da disposição do sistema em termos de comprimento do tubo, acessórios, diâmetro do tubo, alteração na elevação do líquido, pressão sobre a superfície do líquido etc.
Informe se é verdadeiro (V) ou falso (F) o que se afirma abaixo sobre sistemas de bombas.
( ) O NPSHD (disponível) é influenciado por quatro variáveis resultantes do sistema no qual a bomba irá operar. Essas quatro variáveis estão sob controle do fabricante e, portanto, devem ser consultadas.
( ) O NPSHR (requerido) é resultante do projeto da bomba e é controlado apenas pelo fabricante. O fabricante da bomba deverá saber informar o NPSH requerido por suas bombas operando em determinadas condições.
( ) Todas as bombas que trabalham livre de cavitação respeitam a seguinte regra: NPSHD > NPSHR.
A alternativa que apresenta a sequência correta é
A equação de Bernoulli descreve o comportamento de um fluido que se move ao longo de um tubo ou conduto, podendo ser utilizada para calcular a velocidade da água.
A equação pode ser escrita: 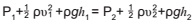 , em que:
, em que:
υ = velocidade do fluido ao longo do conduto.
g = aceleração da gravidade.
h = altura em relação a um referencial.
P = pressão ao longo do recipiente.
ρ = massa específica do fluido.
Considerando que uma represa retira a água em um grande lago artificial, sabe-se que o volume retirado é insignificante. Assim sendo, se a barragem tem um pequeno buraco a 1,4m abaixo da superfície do lago, a que velocidade a água sai do buraco?
O balanço de massa representa uma peça fundamental do projeto de equipamentos e torna-se complexo quando tratamos de processos constituídos por diversos equipamentos interligados. Tal complexidade aumenta em sistemas multifásicos, heterogêneos e com reações químicas.
Analise as assertivas abaixo.
I. Um sistema pode ser denominado fechado quando não existe fluxo de massa através de suas fronteiras; e aberto quando a massa flui através das fronteiras do mesmo.
II. A partir do balanço de massa, podem ser obtidas tantas equações, quantos forem os componentes do processo.
III. O tempo investido na coleta e compreensão de informações do problema previne o tempo gasto com correção ou reinício do mesmo.
IV. Na operação em regime estacionário, os valores das variáveis de processo variam com o tempo em alguma posição fixa do processo.
Está correto apenas o que se afirma em
Analise as Leis da Termodinâmica relacionadas por PW Atkins (2009), em seu livro Físico‐Química.
I. A entropia do universo tende a aumentar.
II. A energia interna de um sistema isolado é constante.
III. A velocidade de variação de momento é igual à força.
IV. As entropias de todas as substâncias perfeitamente cristalinas são as mesmas em T = 0.
É descrita como a Segunda Lei da Termodinâmica apenas a afirmativa
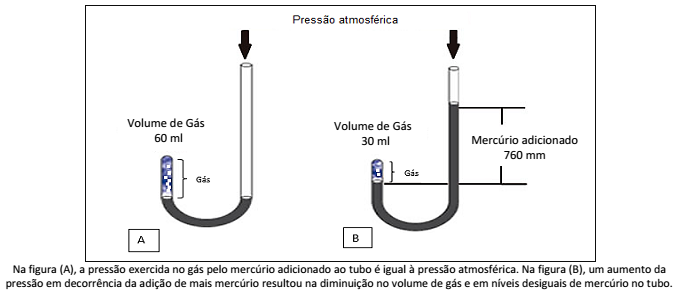
Essa imagem evidencia a relação inversa existente entre a pressão e o volume. Essa teoria se aplica à lei (de):
“A termodinâmica química estuda, entre outras coisas, as mudanças de energia que acompanham as reações químicas.”
(Fundamentos de Química Experimental, Maurício Gomes Constantino.)
Em relação à termoquímica, marque V para as afirmativas verdadeiras e F para as falsas.
( ) A máxima quantidade de energia que um sistema químico pode produzir é medida pela variação de energia livre: ΔG.
( ) Na entalpia da transformação, as medidas são geralmente efetuadas não mantendo uma pressão constante e é representada como ΔH.
( ) Uma reação na qual o calor é absorvido (a temperatura da mistura de reação diminui quando reage) é chamada de endotérmica e o ΔH é positivo.
( ) Uma reação na qual o calor é perdido pelos reagentes para o meio ambiente (a temperatura da mistura de reação aumenta quando reage) é dita exotérmica, onde ΔH é negativo.
A sequência está correta em
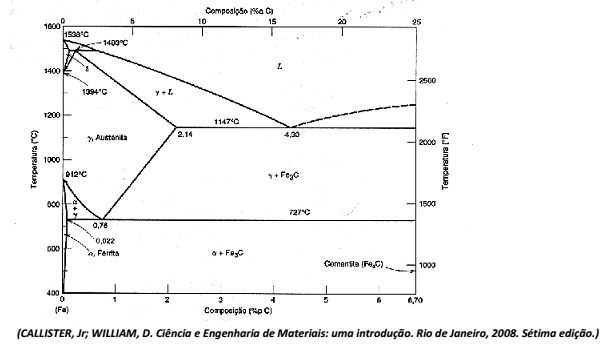
Para um aço contendo 81% de perlita, as porcentagens de ferrita e cementita são, respectivamente:
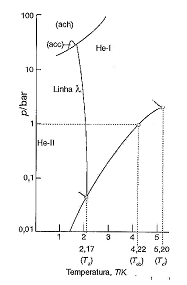
Sobre o diagrama de fases do hélio (4He), analise as afirmativas a seguir.
I. A linha λ assinala as condições para as quais a fase líquida e a fase sólida do hélio estão em equilíbrio. II. O He-II é um superfluido. III. As identificações ach e acc referem-se a fases sólidas distintas com estruturas diferentes do agrupamento dos átomos: uma delas é o agrupamento compacto hexagonal, ach; e a outra, o agrupamento compacto cúbico, acc.
Está(ão) correta(s) apenas a(s) afirmativa(s)
O estado mais simples da matéria é um gás, uma forma da matéria que ocupa qualquer recipiente que a contenha. É conveniente imaginar um gás como um conjunto de moléculas em movimento permanente e aleatório, com velocidades médias que aumentam quando a temperatura se eleva. Um gás difere de um líquido pelo fato de ter suas moléculas muito separadas umas das outras. Sobre os gases, marque V para as afirmativas verdadeiras e F para as falsas.
( ) O tamanho das moléculas é desprezível no sentido de que seus diâmetros são muito menores do que a distância média percorrida entre as colisões.
( ) Um gás real tem o comportamento tanto mais semelhante ao de um gás perfeito quanto mais alta for a pressão.
( ) A velocidade média quadrática das moléculas de um gás é proporcional à raiz quadrada da temperatura e à raiz quadrada da massa molar.
( ) As leis de Boyle e de Charles são exemplos de uma lei limite.
A sequência está correta em
Alguns fatores ocorrem naturalmente, outras não. Um gás, por exemplo, se expande até ocupar todo o volume disponível que lhe é oferecido. Um corpo quente se resfria até atingir a temperatura das suas vizinhanças, e uma reação química avança preferencialmente num sentido e não no sentido inverso. O reconhecimento da existência de duas classes de processos, os espontâneos e os não espontâneos, é resumido pela Segunda Lei da Termodinâmica. Sobre o tema, analise as afirmativas a seguir.
(Considere: ln 2 = 0,69.
ln 2,8 = 1,03.)
I. A variação de entropia de um gás perfeito quando ele se expande isotermicamente do volume Vi até o volume Vf é 8,62 JK–1
II. A variação de entropia do argônio, que está inicialmente a 25°C e 1,00 bar, num recipiente de 0,500 dm3 de volume e que se expande até o volume de 1,000 dm3 , sendo simultaneamente aquecido até 100°C é 0,173 JK–1 .
III. Num ciclo termodinâmico, a variação global de uma função de estado (do estado inicial até o estado final e então de volta para o estado inicial) é igual a zero.
Está(ão) correta(s) apenas a(s) afirmativa(s)