Questões Militares
Para engenharia química
Foram encontradas 255 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Analise a equação a seguir.
ΔU = q + w
A primeira Lei da Termodinâmica estabelece que a energia
interna de um sistema pode ser expressa pela equação acima.
Com base nos princípios da Termodinâmica e nessa equação,
assinale a opção correta.
Um mol de gás hidrogênio, a 27 °C em um sistema fechado, se expande isotermicamente contra uma pressão externa constante igual a 1 atm, até duplicar o seu volume inicial. Qual é o calor necessário para manter constante a temperatura do gás, sabendo que a pressão final do gás é 1 atm?
Dados : ΔU = Q - W
W = PextΔV
PV = nRT
T(K) = T(°C) + 273
R = 0,082 atm•L • mol-1 • K-1
1atm = 105 N • m-2
Ferro e manganês são elementos amplamente utilizados nos processos de fabricação de ligas de aço e, por isso, possuem grande importância industrial e tecnológica. O diagrama mostra as fases em equilíbrio do sistema Fe-Mn para diferentes temperaturas e concentrações.
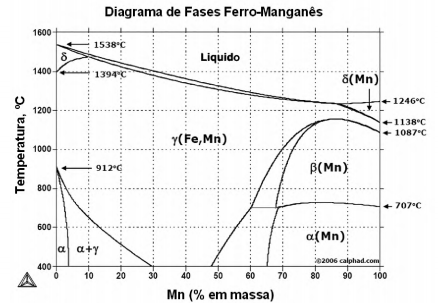
Analise as seguintes afirmações retiradas do diagrama de fases acima.
I. A temperatura liquidus do ferro puro é maior que a do manganês puro.
II. Uma liga com 95% de manganês a 1200°C possui uma fase isenta de ferro.
III. Na temperatura de 912°C ocorre uma transformação eutetoide.
IV. Independentemente do percentual de Mn, a 1000°C o material estará no estado sólido.
Estão corretas apenas as afirmativas
A figura apresentada a seguir representa um diagrama de equilíbrio de fases (hipotético) das ligas A-B.
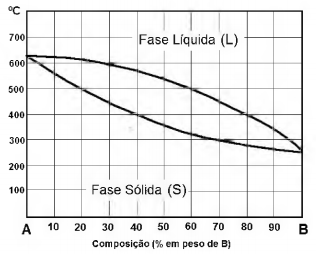
Uma determinada peça composta da liga A-B foi aquecida em condições de equilíbrio até a temperatura de 500°C e
fundiu parcialmente. Sabendo que nesta temperatura a fase sólida possui 80kg do elemento químico B e a fase
líquida possui 40kg do elemento químico A, qual é a percentagem em peso de B da liga que compõe essa peça?
A figura apresentada a seguir representa um diagrama de equilíbrio de fases (hipotético) das ligas A-B. Na temperatura de 250°C a solubilidade de equilíbrio do elemento químico B na fase sólida α é igual a 98% .
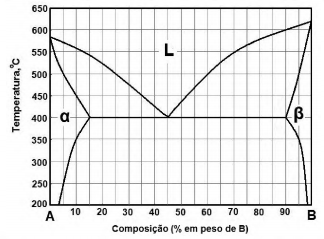
Uma peça de massa 600kg e com 25% em peso de B em sua composição foi resfriada em condições de equilíbrio até a temperatura de 250°C. Calcule a massa, em kg, de faze β precipitada dentro do microconstituinte α primário.
Considere as supostas variações de entropia (∆S) nos processos abaixo:
I) cristalização do sal comum (∆S > 0)
II) sublimação da naftalina (naftaleno ) ( ∆S > 0)
III) mistura de água e álcool ( ∆S < 0)
IV) ferro (s) ferro (l) ( ∆S > 0)
ferro (l) ( ∆S > 0)
V) ar 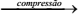 ar comprimido (∆S < 0)
ar comprimido (∆S < 0)
As variações de entropia indicadas nos processos que estão corretas são:
FOLHA DE DADOS
Massas Atômicas (u):
O = 16
C = 12
S = 32
H = 1
Na = 23
Ni = 59
Ag = 108
U = 238
Dados Termodinâmicos:
R = 0,082 atm.L.mol-1.K-1 = 8,314 J.mol-1K-1
Um gás ideal sofre uma mudança de estado ilustrada pelos gráficos I e II abaixo.
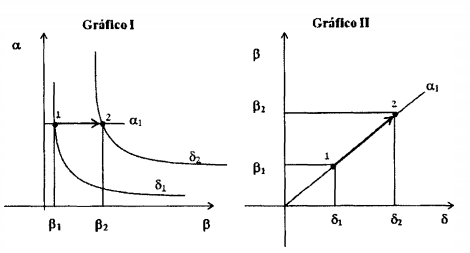
Dentre as alternativas abaixo, assinale aquela que se ajusta aos gráficos acima.
FOLHA DE DADOS
Massas Atômicas (u):
O = 16
C = 12
S = 32
H = 1
Na = 23
Ni = 59
Ag = 108
U = 238
Dados Termodinâmicos:
R = 0,082 atm.L.mol-1.K-1 = 8,314 J.mol-1K-1
Em sistemas envolvendo reações paralelas, um importante parâmetro é a seletividade (se), definida como a razão entre as taxas de geração dos produtos de interesse (I) e dos secundários (S).
Considere o caso em que a taxa de produção de I é dada por 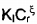 e a de S por
e a de S por 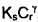 , onde:
, onde:
• Cr é a concentração do reagente;
• KI e Ks são as velocidades específicas de reação para I e S, respectivamente;
• 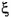 e γ são dois números inteiros e positivos.
e γ são dois números inteiros e positivos.
Para uma temperatura constante, pode-se afirmar que a seletividade:
FOLHA DE DADOS
Massas Atômicas (u):
O = 16
C = 12
S = 32
H = 1
Na = 23
Ni = 59
Ag = 108
U = 238
Dados Termodinâmicos:
R = 0,082 atm.L.mol-1.K-1 = 8,314 J.mol-1K-1
A variação de entropia de um sistema fechado constituído por um gás ideal, quando sofre uma transformação, pode ser calculada pela expressão genérica:
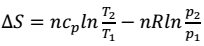
em que os subscritos 1 e 2 representam dois estados quaisquer. Assinale a única afirmativa correta.
O dispositivo a seguir utiliza a radiação solar para quantificar variações em propriedades termodinâmicas.
Este dispositivo é composto por uma lente convergente e por um porta-amostras. A lente possui área útil
de 80,0 cm2
, absortividade (α) de 20% e transmissividade 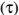 de 80%. O porta-amostras possui
absortividade de 100% e volume variável, operando à pressão constante de 1,0 atm.
de 80%. O porta-amostras possui
absortividade de 100% e volume variável, operando à pressão constante de 1,0 atm.
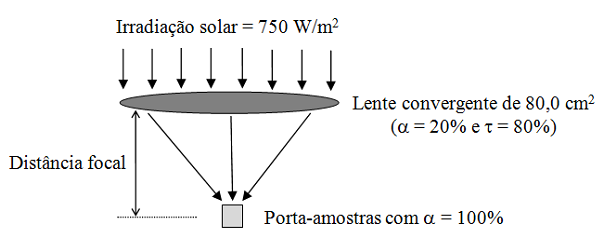
Em um procedimento experimental, injetou-se 0,100 mol de uma substância pura líquida no porta-amostras
do dispositivo. Em seguida, mediu-se um tempo de 15,0 min para a vaporização total da
amostra, durante o qual a irradiação solar permaneceu constante e igual a 750 W/m2
. Nesse processo, a
temperatura do porta-amostras estabilizou-se em 351 K. No experimento, o calor sensível da amostra e a
radiação emitida pelo porta-amostras são desprezíveis. Pode-se concluir que na vaporização total da
substância, as variações de entalpia molar padrão e de entropia molar padrão são, respectivamente:
Um tambor selado contém ar seco e uma quantidade muito pequena de acetona líquida em equilíbrio dinâmico com a fase vapor. A pressão parcial da acetona é de 180,0 mm Hg e a pressão total no tambor é de 760,0 mm Hg.
Em uma queda durante seu transporte, o tambor foi danificado e seu volume interno diminuiu para 80% do volume inicial, sem que tenha havido vazamento. Considerando-se que a temperatura tenha se mantido estável a 20 °C, conclui-se que a pressão total após a queda é de:
DADOS:
Valores de tangente:
tan(0°) = 0, tan(30°) = (√3)/3, tan(45°) = 1, tan(60°) = √3, tan(90°) = ∞, tan(180°-α) = -tan(α), tan(-α) = -tan(α).
Valores de seno:
sen(0°) = 0, sen(30°) = 1/2, sen(45°) = (√2)/2, sen(60°) = (√3)/2, sen(90°) = 1, sen(90°-α) = cos(α), sen(180°-α) = sen(α), sen(-α) = -sen(α).
Valores de cosseno:
cos(0°) = 1, cos(30°) = (√3)/2, cos(45°) = (√2)/2, cos(60°) = 1/2, cos(90°) = 0, cos(90°-α ) = sen(α), cos(180°-α) = -cos(α), cos(-α) = cos(α).
Transformada de Laplace:
L{f(t)} = F(s), L{exp(-at)} = 1/(s+a), L{1 - exp(-at)} = a/(s(s+a)), L{cos(at)} = s/(s2 +a2 ), L{sen(at)} = a/(s2 +a2).
Resistividade aproximada dos condutores de cobre:
seção transversal de 1,5 mm2 = 10 Ω/km, seção transversal de 2,5 mm2 = 7 Ω/km,
seção transversal de 4 mm2 = 4 Ω/km, seção transversal de 6 mm2 = 3 Ω/km.
Representação de número complexo em forma polar: a∠b onde a é o módulo e b o argumento.
Representação do complemento do valor A: Ā
Um sistema linear invariante no tempo tem a seguinte função característica
s3 + 3 s2 + 3 s + K = 0, onde K é uma variável de controle.
Analise a estabilidade do sistema e assinale a alternativa correta.
DADOS:
Valores de tangente:
tan(0°) = 0, tan(30°) = (√3)/3, tan(45°) = 1, tan(60°) = √3, tan(90°) = ∞, tan(180°-α) = -tan(α), tan(-α) = -tan(α).
Valores de seno:
sen(0°) = 0, sen(30°) = 1/2, sen(45°) = (√2)/2, sen(60°) = (√3)/2, sen(90°) = 1, sen(90°-α) = cos(α), sen(180°-α) = sen(α), sen(-α) = -sen(α).
Valores de cosseno:
cos(0°) = 1, cos(30°) = (√3)/2, cos(45°) = (√2)/2, cos(60°) = 1/2, cos(90°) = 0, cos(90°-α ) = sen(α), cos(180°-α) = -cos(α), cos(-α) = cos(α).
Transformada de Laplace:
L{f(t)} = F(s), L{exp(-at)} = 1/(s+a), L{1 - exp(-at)} = a/(s(s+a)), L{cos(at)} = s/(s2 +a2 ), L{sen(at)} = a/(s2 +a2).
Resistividade aproximada dos condutores de cobre:
seção transversal de 1,5 mm2 = 10 Ω/km, seção transversal de 2,5 mm2 = 7 Ω/km,
seção transversal de 4 mm2 = 4 Ω/km, seção transversal de 6 mm2 = 3 Ω/km.
Representação de número complexo em forma polar: a∠b onde a é o módulo e b o argumento.
Representação do complemento do valor A: Ā
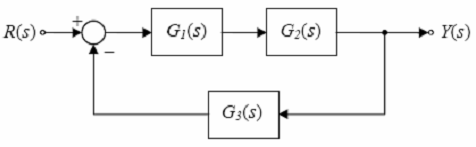
Considere o sistema linear invariante no tempo colocado na figura a seguir, onde as variáveis mostradas foram obtidas por transformada de Laplace. A função de transferência Y(s)/R(s) é